
| A. | 碘乙烷水解实验后,取水解液,加入AgNO3溶液,检验卤素离子 | |
| B. | 碘乙烷水解实验后,取水解液,加入KMnO4(H+)溶液,检验产物乙醇 | |
| C. | 碘乙烷消去实验后,将气体导入KMnO4(H+)溶液,检验产物乙烯 | |
| D. | 碘乙烷消去实验后,将气体导入Br2(CCl4)溶液,检验产物乙烯 |
分析 A.碘乙烷水解实验后检验卤素离子,应先加酸至酸性,再加入AgNO3溶液检验;
B.碘乙烷水解实验后生成醇和HI,HI具有强还原性;
C.碘乙烷消去实验后,生成乙烯,但乙醇易挥发,乙烯、乙醇均能被高锰酸钾氧化;
D.碘乙烷消去实验后,生成乙烯,乙醇易挥发,但乙醇不与溴反应.
解答 解:A.碘乙烷水解实验后检验卤素离子,应先加酸至酸性,再加入AgNO3溶液检验,则没有加酸中和碱,实验不能成功,故A错误;
B.碘乙烷水解实验后生成醇和HI,HI具有强还原性,没有先除去HI,不能检验乙醇,实验不能成功,故B错误;
C.碘乙烷消去实验后,生成乙烯,但乙醇易挥发,乙烯、乙醇均能被高锰酸钾氧化,应先排除乙醇的干扰,实验不能成功,故C错误;
D.碘乙烷消去实验后,生成乙烯,乙醇易挥发,但乙醇不与溴反应,则气体导入Br2(CCl4)溶液,可检验产物乙烯,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的结构与性质、有机物的检验等,把握卤代烃的水解、消去反应实验及发生的反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
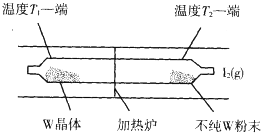 利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0
利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0查看答案和解析>>
科目:高中化学 来源: 题型:解答题
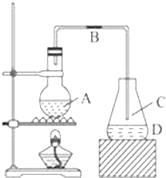 某化学课外小组用如图装置制取溴苯,请按要求完成下列小题:
某化学课外小组用如图装置制取溴苯,请按要求完成下列小题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
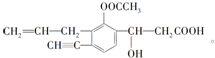
 +NaHCO3→
+NaHCO3→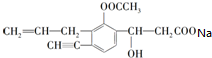 +CO2↑+H2O.
+CO2↑+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫有漂白性,常用作棉、麻、纸张和食品的漂白 | |
| B. | 大量使用化肥和农药,以提高农作物产量 | |
| C. | 汽车排放的尾气中含有NO、CO2等大气污染物 | |
| D. | 安装煤炭“固硫”装置,可以降低酸雨发生率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测现象不一致的是( )| 选项 | ①中物质 | ②中物质 | 预测①中现象 |
| A | 酚酞溶液 | 浓氨水 | 无色变红色 |
| B | 湿润红布条 | 饱和氯水 | 红布条褪色 |
| C | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
| D | 硝酸银溶液 | 浓盐酸 | 有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有七个主族,八个副族 | |
| B. | IA族的元素全部是金属元素 | |
| C. | 元素周期表的第三列(从左往右)所含元素种类最多 | |
| D. | 元素周期表有三个长周期(均含18种元素),三个短周期(均含8种元素) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 元素周期表可以指导我们寻找和合成成新的物质,如金属和非金属分界线附近的元素可用于制造半导体材料,是科学研究的热点
元素周期表可以指导我们寻找和合成成新的物质,如金属和非金属分界线附近的元素可用于制造半导体材料,是科学研究的热点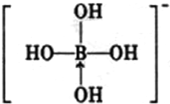 或
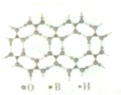
或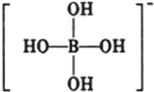 ,硼酸具有层状结构,每层结构如图所示,每摩尔晶体中所含氢键的数目为3NA(设NA为阿伏伽德罗常数的值)
,硼酸具有层状结构,每层结构如图所示,每摩尔晶体中所含氢键的数目为3NA(设NA为阿伏伽德罗常数的值)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com