下列说法正确的是( )
A.镁与极稀硝酸反应生成硝酸铵的离子方程式为:4Mg+6H++NO3-=4Mg2++NH4++3H2O
B.25℃时,将20 mL 0.1mol?L-1H2SO4溶液和30 mL 0.15mol?L-1NaOH溶液混合,若混合后溶液体积不变,则混合溶液的pH为11
C.将10 mL 0.1 mol?L-1KAI(SO4)2溶液和10 mL0.2 mol?L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1:2
D.浓度均为0.1 mol?L-1的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
【答案】
分析:A.离子反应中应遵循电荷守恒;
B.碱过量,过量的c(OH
-)=
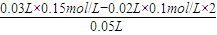
=0.01mol/L;
C.KAl(SO
4)
2、Ba(OH)
2溶的物质的量之比为1:2,反应生成硫酸钡、偏铝酸钾、水;
D.电荷守恒式为c(Na
+)+c(H
+)=c(CH
3COO
-)+c(OH
-),物料守恒式为c(CH
3COOH)+c(CH
3COO
-)=2c(Na
+).
解答:解:A.离子反应中应遵循电荷守恒,则镁与极稀硝酸反应生成硝酸铵的离子方程式为4Mg+10H
++NO
3-=4Mg
2++NH
4++3H
2O,故A错误;
B.碱过量,过量的c(OH
-)=
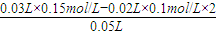
=0.01mol/L,所以混合溶液的pH为12,故B错误;
C.KAl(SO
4)
2、Ba(OH)
2溶的物质的量之比为1:2,反应生成硫酸钡、偏铝酸钾、水,该反应中不生成氢氧化铝沉淀,故C错误;
D.电荷守恒式为c(Na
+)+c(H
+)=c(CH
3COO
-)+c(OH
-),物料守恒式为c(CH
3COOH)+c(CH
3COO
-)=2c(Na
+),所以c(CH
3COOH)+2c(H
+)=c(CH
3COO
-)+2c(OH
-),故D正确;
故选D.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解本题的关键,注意计算反应物的物质的量的关系来判断生成物及溶液的酸碱性,题目难度中等.

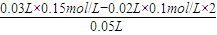 =0.01mol/L;
=0.01mol/L;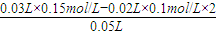 =0.01mol/L,所以混合溶液的pH为12,故B错误;
=0.01mol/L,所以混合溶液的pH为12,故B错误;

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,