
把氮气和氢气以1∶1的物质的量比混匀后分成四等分,分别同时充入A、B、C、D四个装有催化剂的真空容器中(容器的容积固定),在保持相同的温度的条件下,四个容器中的合成氨反应相继达到化学平衡状态.分析表中实验数据后回答问题(用A、B、C、D填空).

(1)都达到平衡时,________容器中NH3的物质的量所占的比例最大.
(2)达到平衡时所需时间最长的容器是________.
(3)四个容器容积由小到大的排列顺序是________.
科目:高中化学 来源: 题型:阅读理解
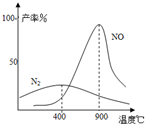 (2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下:
(2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下: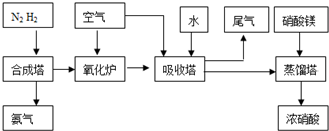
| 时间(h)浓度(mol/L) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0 | 0.200 | 0.600 | C3 | C3 |
| 1 |
| a |
| 1 |
| a |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)反应前后的压强之比。
(2)平衡时混合气体的平均相对分子质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
把氢气和氮气以1∶1的物质的量之比放入一容积固定的容器中,测得平衡时氮气的转化率为20%时,求:
(1)反应前后的压强之比。
(2)平衡时混合气体的平均相对分子质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)把氮气和氢气以1:1的物质的量之比均匀混合后分成四等份,分别充入A、B、C、D四个装有催化剂的固定体积的真空容器中,在保持相同温度的条件下,四个容器中的合成氨反应相继达到化学平衡状态。有关实验数据如下表所示:
| A | B | C | D |
平衡时混合物的平均分子量 |
|
| 16 | 17 |
平衡时N2的转化率 | 20% |
|
|
|
平衡时H2的转化率 |
| 30% |
|
|
(1)合成氨反应的平衡常数的表达式为 ,若用KA表示一定条件下容器A中所进行反应的平衡常数,容器B、C、D依此类推。则在题目所述的条件下,KA、KB、KC、KD之间的大小关系是 。
(2)当四个容器中进行的反应都达到平衡时, 容器中的氨气的物质的量所占的比例最大。
(3)达到平衡时所需时间最长的容器是 。
(4)四个容器容积由小到大的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com