
按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物—酸—碱—盐”顺序排列的是
A.H2O、HNO3、NaOH、KNO3
B.CO2、H2CO3、Na2CO3、Ca(HCO3)2
C.H2SO4、HCl、Mg(OH)2、MgCl2
D.SO3、NaHCO3、NaOH、Na2SO4
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年江西八一、洪都、麻丘中学等高二上期中联考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.自发反应的熵一定增大,非自发反应的熵一定减小或不变
C.ΔH<0、ΔS<0的反应一定能自发进行
D.ΔH>0、ΔS<0的反应一定不能自发进行
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期期中阶段测试化学试卷(解析版) 题型:选择题
下列事实所对应的方程式不正确的是(反应条件已略去)
A.盛放氢氧化钠溶液的试剂瓶不能用玻璃塞:SiO2 + 2NaOH = Na2SiO3 + H2O
B.高温下铁与水蒸气反应生成保护膜:2Fe + 6H2O(g) = 2Fe(OH)3 + 3H2↑
C.工业制取漂粉精:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
D.实验室制取氨气:2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑+ 2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:填空题
空气中CO2的含量及有效利用,已经引起各国的普遍重视
Ⅰ: 目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ,△H=-49.0kJ/mol;测得CO2和CH3OH(g)的浓度随时间变化如图甲所示。
CH3OH(g)+H2O(g) ,△H=-49.0kJ/mol;测得CO2和CH3OH(g)的浓度随时间变化如图甲所示。
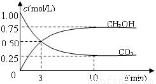
(1)前3min内,平均反应速率v(H2)= mol·L-1·min-1。此温度下该反应的平衡常数为 (保留两位小数,注意要写单位)。
(2)下列措施中,既能使反应加快,又能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入惰性气体
C.将H2O(g)从体系中分离 D.再充入1mol H2
(3)图乙中t5时引起平衡移动的条件是 。(填序号)
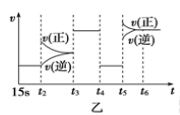
A.升高温度 B.增大反应物浓度 C.使用催化剂 D.增大体系压强
(4)反应达到平衡后,若向反应体系再加入CO2(g)、H2(g) 、CH3OH(g)、H2O(g)各1mol,化学平衡 (填“正向”、“逆向”或“不”)移动。
Ⅱ:利用CO2(g)+CH4(g) 2CO(g)+2H2(g)将CO2转化成燃料气。T℃时,在恒容密闭容器中通入物质的量均为0.1 mol的CH4与CO2,发生上述反应,吸收热量Q1kJ,测得CH4的平衡转化率与温度及压强的关系如图所示
2CO(g)+2H2(g)将CO2转化成燃料气。T℃时,在恒容密闭容器中通入物质的量均为0.1 mol的CH4与CO2,发生上述反应,吸收热量Q1kJ,测得CH4的平衡转化率与温度及压强的关系如图所示
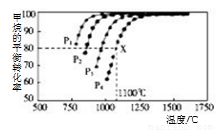
(5)下列事实能说明该反应达到平衡的是( )
a.CO的物质的量不再发生变化
b.混合气体的密度不再发生变化
c.v正(CO2)= 2v逆(H2)
d.混合气体压强不再发生变化
e.单位时间内生成n mol CH4的同时消耗2n mol H2
(6)据图可知P1、P2、P3、P4由小到大的顺序是 。
(7)若将上述容器改为恒压容器(反应前体积相同),起始时通入物质的量均为0.1 mol的CH4与CO2,相同的温度下充分反应达到平衡后,放出热量Q2 kJ,
则Q1 Q2(填 “>”“=”或“<”)
Ⅲ: 设反应①Fe(s)+CO2(g) FeO(s)+CO(g) 和反应②Fe(s)+H2O(g)
FeO(s)+CO(g) 和反应②Fe(s)+H2O(g) FeO(s)+H2(g)的平衡常数分别为K1、K2,在不同温度下, K1、K2的值如下表所示:
FeO(s)+H2(g)的平衡常数分别为K1、K2,在不同温度下, K1、K2的值如下表所示:
T(K) | K1 | K2 |
973 | 1.47 | 2.36 |
1173 | 2.15 | 1.67 |
(8)现有反应CO2(g)+H2(g) CO(g)+H2O(g),是 (填“吸”或“放”)热反应。
CO(g)+H2O(g),是 (填“吸”或“放”)热反应。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省四地六校高二上学期11月联考化学试卷(解析版) 题型:选择题
如图所示,利用2Ag + Cl2 = 2AgCl设计的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质)。下列分析不正确的是

A.空气中c(Cl2)越大,Ag极消耗速率越快
B.Ag+向Pt电极移动
C.电子由Ag电极经外电路流向Pt电极
D.Ag电极上发生了还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二上学期期中测试化学试卷(解析版) 题型:选择题
恒温下,反应aX(g) bY(g) + cZ(g) 达到平衡状态,把容器体积压缩到原来的1/2,且达到新的平衡状态时,X的物质的量浓度从0.1mol/L增大到0.19mol/L,下列判断正确的是
bY(g) + cZ(g) 达到平衡状态,把容器体积压缩到原来的1/2,且达到新的平衡状态时,X的物质的量浓度从0.1mol/L增大到0.19mol/L,下列判断正确的是
A.a>b+c B.a<b+c C.a=b+c D.a=b=c
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一上学期期中测试化学试卷(解析版) 题型:选择题
24mL浓度为0.05mol/L 的Na2SO3溶液恰好与20mL浓度为0.02 mol/L的K2Cr2O7溶液完全反应;已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A、+2 B、+3 C、+4 D、+5
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第二次联考化学试卷(解析版) 题型:选择题
a mol FeS与b mol FeO投入到V L c mol·L-1的硝酸溶液中,恰好完全反应,还原产物只有NO,所得澄清溶 液可看作是Fe(NO3)
液可看作是Fe(NO3) 3与H2SO4的混合液,则反应中未被还原的硝酸可能为
3与H2SO4的混合液,则反应中未被还原的硝酸可能为
①(a+b)×63g
②(a+b)×189g
③(a+b)mol
④(Vc-3a-b/3)mol
A.②④ B.②③ C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期第二次月考化学试卷(解析版) 题型:选择题
A、B、C、X均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去),下列说法错误的是
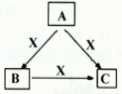
A、若X为Cl2,则C可能为FeCl3
B、若X为KOH溶液,则A可能为AlCl3
C、若X为O2,则A可为硫化氢
D、若A、B、C均为焰色反应呈黄色的物质,则X可能为O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com