
���� ��1������ɫ��ĩ��ˮ�ܽ⣬����ɫ��Һ����һ������FeCl3����K2SO4��BaCl2����ͬʱ���ڣ�
��2����1�������õ���ɫ��Һ�м���NaOH��Һ�����ȣ����۲쵽�а�ɫ����A���ɣ�AӦΪBaCO3�����˺�����Һ�еμ������ữ��AgNO3��Һ���ֵõ���ɫ����B��BΪAgCl����һ����NaHCO3��BaCl2����K2SO4������ȷ���Ƿ�KCl���Դ������
��� �⣺��1��������������֪����ɫ����A�Ļ�ѧʽ��BaCO3����Ӧ��ѧ��Ӧ�����ӷ���ʽ��HCO3-+OH-=CO32-+H2O��CO32-+Ba2+=BaCO3������HCO3-+OH-+Ba2+=H2O+BaCO3������
�ʴ�Ϊ��BaCO3��HCO3-+OH-=CO32-+H2O��CO32-+Ba2+=BaCO3����
��2��������������֪��ԭ��ɫ��ĩ��һ������NaHCO3��BaCl2�����ܺ���KCl���Կ��ܺ��е����ʣ���ͨ����ɫ��Ӧ��һ�����飬
�ʴ�Ϊ��NaHCO3��BaCl2��KCl����ɫ��
���� ���⿼��������ƶϣ�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ������Ϊ���Ĺؼ������ط������ƶ������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16O2��18O2��Ϊͬ���칹�� | |
| B�� | 16O��18O��������Ų���ʽ��ͬ | |
| C�� | ͨ����ѧ�仯����ʵ��16O��18O����ת�� | |
| D�� | ��������H218O��D216O���еĵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��A��=1.0mol/L c��B��=0.2mol/L | B�� | c��B��=0.5mol/L c��C��=1.2mol/L | ||
| C�� | c��A��=0.4mol/L c��C��=1.8mol/L | D�� | c��A��=0.9mol/L c��B��=0.5mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �ۢ� | C�� | �٢� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�������ͭƬ�ϣ�Cu+2H+�TCu2++H2�� | |
| B�� | ��CH3COOH��Һ�м���CaCO3��2CH3COOH+CaCO3�T2CH3COO-+Ca2++H2O+CO2�� | |
| C�� | ϡ������Ba��OH��2��Һ��ϣ�H++SO42-+OH-+Ba2+�TBaSO4��+H2O | |
| D�� | NaOH��Һ��KHCO3��Һ��ϣ�OH-+HCO3-�TH2O+CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
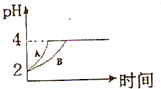 ����������Ũ�Ⱦ�Ϊ1��10-3mol/L�ļ�����Һ�������ᡢ�ڴ��ᡢ�۰�ˮ����NaOH��Һ���ش��������⣺
����������Ũ�Ⱦ�Ϊ1��10-3mol/L�ļ�����Һ�������ᡢ�ڴ��ᡢ�۰�ˮ����NaOH��Һ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3- | B�� | NO3- | C�� | H+ | D�� | Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ӳɷ�Ӧ | B�� | �ۺϷ�Ӧ | C�� | ȡ����Ӧ | D�� | ������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۡ�CuO��HClO��Cu | |
| B�� | ˮ������Na2O��CaO•6SiO2��AgO��SO3 | |
| C�� | KAl ��SO4�� 2•12H2O��KCIO3��NH3•H2O��CH3CH2OH | |
| D�� | ��ͨ������H2O��Fe ��SCN�� 3�������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com