
��9�֣����ӡ�ÿ���������桷�ع��˺ӱ�ʡһЩ������ҵ��Ƥ����ϰ��Ƴɹ�ҵ���������۸��㽭����ijЩ��ҩ��ҵ�����ձ��ҩ�ý��ҽ��뻼�߸��С�������ˮ���Ե����ʻ�������ˮ�γɽ��塣�ɹ�ҵ�����ƳɵĽ����������г�����ؽ���Cr���Ӷ�����������˺���
��1����֪Fe(CrO2)2�и�Ԫ����+3�ۣ���������Ԫ���� �ۡ�CrO2����һ��������ӣ���Fe(CrO2)2����__________����ᡱ����������Ρ������������������ˮ��Һ��K2SO4��Һ��ͬ�߱��������� ��
a�������ȶ����ܷ���ó���
b�����߾��ж��������
c����ɢ�����ӿ�ͨ����ֽ
��2����֪CN�����ӡ�SCN�����Ӻ�Cl������������֮���������(CN)2���������(SCN)2��������Cl2Ҳ������֮�����ҳ��³�ѹ��Ϊ���壬������з�Ӧ����ʽ��
��MnO2��HSCN��Ũ��Һ���ȵĻ�ѧ����ʽ��ʽ�� ��
��(CN)2��NaOH��Һ��Ӧ�����ӷ�Ӧ����ʽ�� ��
��3����֪H2O2�Ƕ�Ԫ���ᡢ��д��H2O2��Ca(OH)2��Һ��Ӧ������ʽ�εĻ�ѧʽ ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016������������ѧ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ������
(15 �֣��������ȣ�ClO2������ɫ������ˮ�����壩�Ǹ�Ч���Ͷ���������������Ҫ�����������}��
��1����ҵ�Ͽ���KC1O3��Na2SO3��H2SO4�������Ƶ�ClO2���÷�Ӧ�������뻹ԭ�����ʵ���֮��Ϊ ��3�֣���
��2��ʵ������NH4Cl�����ᡢNaClO2(�������ƣ�Ϊԭ�ϣ�ͨ�����¹����Ʊ�ClO2��
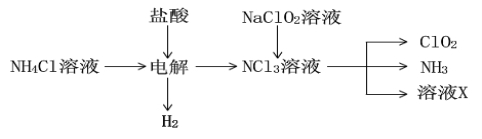
�ٵ��ʱ������Ӧ�Ļ�ѧ����ʽΪ ��3�֣���
����ҺX�д������ڵ���������__________________��
�۳�ȥClO2�е�NH3��ѡ�õ��Լ��� (����)��
a��ˮ b����ʯ�� c��Ũ���� d������ʳ��ˮ
��3��Ϊ�˲ⶨ���������ClO2�ĺ���������ͨ�����ữ��KI��Һ��֮��Ӧ��
����д��ClO2��⻯�ط�Ӧ�����ӷ���ʽΪ ��3�֣���
�������Ӧ�����й������� 0.04 mol��KI����˻��������ClO2������Ϊ________�ˡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ�ڵ�һ�ζ��п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾˮ������ӷ���ʽ��ȷ����
A��CH3COO�� + H2O CH3COOH + OH��
CH3COOH + OH��
B��NH4+ + H2O NH4OH + H+
NH4OH + H+
C��S2�� + 2H2O H2S+2OH��
H2S+2OH��
D��HCO3�� + H2O  H3O++CO32��
H3O++CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ������
�ϳɰ��������о�����Ҫ���⣬Ŀǰ��ҵ�ϳɰ���ԭ��Ϊ��
N2(g)+3H2(g)  2NH3(g) ��H=-93��0kJ/mol
2NH3(g) ��H=-93��0kJ/mol
ij�¶��£���2 L�ܱ������з���������Ӧ�������������
ʱ��/h ���ʵ���/mol | 0 | 1 | 2 | 3 | 4 |
N2 | 2��0 | 1��83 | 1��7 | 1��6 | 1��6 |
H2 | 6��0 | 5��49 | 5��1 | 4��8 | 4��8 |
NH3 | 0 | 0��34 | 0��6 | 0��8 | 0��8 |
��0~2 h�ڣ�v��N2��= ��
��ƽ��ʱ��H2��ת����Ϊ_________________
���������¶Ⱥ�������䣬��ʼͶ���N2��H2��NH3�����ʵ����ֱ�Ϊa mol��b mol��c mol���ﵽƽ���NH3�ȵ�Ũ�����ϱ�����ͬ��Ϊ ����ѡ����ĸ����
A��a=l��b=3��c=0 B��a=4��b=12��c=0
C��a=0��b=0��c=4 D��a=l��b=3��c=2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ�ϳ�����CO��SO2��Ӧ���ɹ�̬S���ʺ�CO2���Ӷ���������������Դ�������Ⱦ��2CO��g��+SO2��g�� 2CO2��g��+S��s����H=��a kJ/mol��a��0��������������ȷ����
2CO2��g��+S��s����H=��a kJ/mol��a��0��������������ȷ����
A���÷�Ӧ��ƽ�ⳣ������ʽΪK=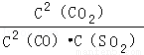
B������Ӧ��ʼʱͶ��2 mol CO�����ƽ��ʱ���ų�����Ϊa kJ
C������ѹǿ�������¶ȶ����Լӿ컯ѧ��Ӧ���ʲ����SO2��ת����
D������λʱ��������2 molCO2��ͬʱ������1mol SO2����˵����Ӧ�ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ��10��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ2����ֽƬ���䵽ͼ1�У��ɵõ�һ��������������ԭ��Ӧ�����ӷ���ʽ(δ��ƽ)�����жԸ÷�Ӧ��˵������ȷ����
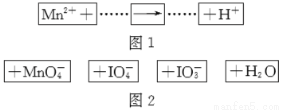
A��IO4����������
B������1 mol Mn2+�μӷ�Ӧת��5 mol����
C���������뻹ԭ�������ʵ���֮��Ϊ5��2
D����ƽ��Mn2+��H+�Ļ�ѧ�������ֱ�Ϊ2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��.���ķ���ϩ�������Ժͻ�ѧ�ȶ����϶��������������ϣ��ųơ�����֮����������������ɻ���������������У��ܷ����ϣ�����Ѫ�ܣ���ѩ�壬��ճ���ȡ���ϳ�·������ͼ��ʾ��

д�����л�ѧ��Ӧ����ʽ��
B��C��_______ _________________
C��D��_____________ _
��ʵ������ȡ��ϩ����ʱ�������¶ȹ����ҺѸ�ٱ�ڣ����������д̼�����ζ������SO2��ijͬѧ�������ͼ��ʾ��ʵ��װ����ȷ֤��Ӧ�ƵõĻ�������к�����ϩ��SO2��

�ɹ�ѡ����Լ��������Ը��������Һ����ϡ���ᡢ��Ũ���ᡢ��Ʒ����Һ����ʯ����Һ����NaOH��Һ��
��1����װ������ʢ�ŵ��Լ��ֱ��ǣ���д��ţ���A_________��B_________��C_________��D_________��
��2��װ��B��������__________________��װ��C��������___________________��
��3����˵����������к�SO2��ʵ��������_________ ______��ȷ֤�������������ϩ��ʵ��������____ __��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�����и�����ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ������
��15�֣�ʵ������MnO2��KOH��KClO3Ϊԭ����ȡ������ص�ʵ���������£�
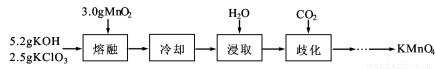
��1������ʱ���������������ƽ�����������ò�����������ԭ���� ��
��2������ʱ��MnO2ת��ΪK2MnO4��KClO3ת��ΪKCl���䷴Ӧ�Ļ�ѧ����ʽΪ ��
��3���������ʵ��ܽ��������ͼ��ʾ��

���绯ʱ��ͨ��CO2��pHΪ10��11��K2MnO4��ɫ��Һת��ΪKMnO4��MnO2���䷴Ӧ�����ӷ���ʽΪ ��
���绯ʱ����ͨ�����CO2��ԭ���� ��
��ͨ��CO2���ò�����պȡ��Һ������ֽ�ϣ��۲쵽 ��֤���绯��Ӧ�ѷ�����
���绯��õ�KMnO4����IJ�������Ϊ���ˡ� �� �����
��4���ڴ�ʵ�������п�ѭ��ʹ�õ����ʵĻ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��һ��ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ħ��������������ȷ����
A��������Ħ��������2��
B��1Ħ���κ����ʵ�����ͨ�����������ʵ�Ħ������
C��1Ħ��H2SO4��������98��/Ħ
D��������Ħ��������1g/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com