
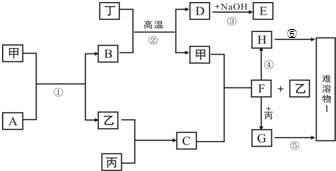
分析 甲、乙、丙、丁为常见单质,其余均为化合物,A是一种常见的液态化合物,则A为H2O,B是具有磁性的氧化物,则B为Fe3O4,D和丁既能和酸反应又能和碱反应,则丁为Al,D为Al2O3,E为NaAlO2,乙在丙中燃烧产生苍白色火焰,则C为HCl,结合转化关系可知,甲为Fe,乙为H2,F为FeCl2,H在空气中很容易被氧化成I,则H为Fe(OH)2,I为Fe(OH)3,G为FeCl3,然后结合物质的性质及化学用语来解答.
解答 解:甲、乙、丙、丁为常见单质,其余均为化合物,A是一种常见的液态化合物,则A为H2O,B是具有磁性的氧化物,则B为Fe3O4,D和丁既能和酸反应又能和碱反应,则丁为Al,D为Al2O3,E为NaAlO2,乙在丙中燃烧产生苍白色火焰,则C为HCl,结合转化关系可知,甲为Fe,乙为H2,F为FeCl2,H在空气中很容易被氧化成I,则H为Fe(OH)2,I为Fe(OH)3,G为FeCl3,
(1)通过以上分析知,B、F分别是Fe3O4、FeCl2,故答案为:Fe3O4;FeCl2;
(2)A+甲反应的化学方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(3)H为Fe(OH)2,I为Fe(OH)3,氢氧化亚铁是白色沉淀、氢氧化铁是红褐色沉淀,氢氧化亚铁不稳定,极易被空气中氧气氧化生成红褐色氢氧化铁沉淀,看到的现象是白色沉淀逐渐变为灰绿色,最终变为红褐色沉淀
,故答案为:白色沉淀逐渐变为灰绿色,最终变为红褐色沉淀;
(4)E是偏铝酸钠,足量二氧化碳通入偏铝酸钠溶液中反应生成氢氧化铝沉淀和碳酸氢钠,离子方程式为CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-,故答案为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-;
(5)将G的饱和溶液滴入沸水中得红褐色液体,该液体是胶体,具有丁达尔效应,其分散质直径在1-100nm之间,能透过滤纸但不能透过半透膜,能和电解质溶液发生聚沉现象,故选AD.
点评 本题考查无机物的推断,把握A、B、D、丁的性质及铝热反应为解答本题的突破口,侧重于金属及其化合物相互转化的考查,知道常见物质特殊性质及铁和水蒸气的反应,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 卤素单质Cl2、Br2、I2的氧化性强弱 | |
| B. | 气态氢化物NH3、H2O、HF的稳定性 | |
| C. | 碱金属单质Li、Na、K与水反应的剧烈程度 | |
| D. | 1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CO2过程中溶液的Kw减小 | |
| B. | 当b=0.2时,所得溶液中部分离子浓度关系为:c (HCO3-)>c (CO32-)>c ( OH-)>c (H+) | |
| C. | b=0.3与b=0.15时,所得溶液中的微粒种类不相同 | |
| D. | 当恰好生成NaHCO3时,溶液中存在:c(Na+)+c(H+)═c(HCO3-)+c( OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量就是物质的质量 | |
| B. | 摩尔是国际单位制七个基本单位之一 | |
| C. | 摩尔是粒子的数量单位 | |
| D. | 阿伏伽德罗常数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③②④① | B. | ③②①④ | C. | ②③①④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | pH=8的NaB溶液中:c(Na+)>c(B-)>c(OH-)>c(H+) | |
| C. | 物质的量浓度相等的①CH3COONH4、②NH4Cl、③NH4HSO4三种溶液中:c(NH4+)大小顺序①=②>③ | |
| D. | 常温下.10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL(反应后溶液的总体积为两反应液体积之和) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2不能与HNO3、H2SO4等所有的酸反应 | |
| B. | CO2和SiO2的对应水化物都是酸,碳酸酸性比硅酸弱 | |
| C. | CO2与SiO2均是酸性氧化物,溶于水均得到相应的酸 | |
| D. | 硅胶常用于做干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某同学利用图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )
某同学利用图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )| X气体 | Y试剂 | Z试剂 | |
| A. | NO2 | H2O | H2O |
| B. | CO2 | H2O | H2O |
| C. | HCl | 饱和食盐水 | 水 |
| D. | NO2和O2 | H2O | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com