

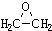
分析 A、D都能与金属钠反应,1mol有机物产生1mol气体,说明A、D中有两个羧基或羟基,D还能与NaHCO3作用产生气体,说明D中有羧基,根据A和D的分子式可知,A为HOCH2CH2OH,D为HOCH2COOH,C可以发生银镜反应,说明C中有醛基,所以C为CH3CHO,B中所有氢原子都有相同的化学环境,则B为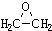 ,据此答题;
,据此答题;
解答 解:A、D都能与金属钠反应,1mol有机物产生1mol气体,说明A、D中有两个羧基或羟基,D还能与NaHCO3作用产生气体,说明D中有羧基,根据A和D的分子式可知,A为HOCH2CH2OH,D为HOCH2COOH,C可以发生银镜反应,说明C中有醛基,所以C为CH3CHO,B中所有氢原子都有相同的化学环境,则B为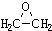 ,
,
(1)A为HOCH2CH2OH,A的名称为 乙二醇,
故答案为:乙二醇;
(2)根据上面的分析可知,A、B的结构简式分别为 HOCH2CH2OH、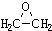 ,
,
故答案为:HOCH2CH2OH、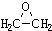 ;
;
(3)比较乙烯与HOCH2COOH的结构可知,HOCH2COOH中得到了三个氧原子,所以由乙烯转化为HOCH2COOH的反应类型为氧化反应,
故答案为:氧化反应;
(4)C为CH3CHO,C发生银镜反应的化学反应方程式CH3CHO+Ag(NH3)2OH$\stackrel{水浴加热}{→}$ CH3COONH4+H2O+2Ag+3NH3↑,
故答案为:CH3CHO+Ag(NH3)2OH$\stackrel{水浴加热}{→}$ CH3COONH4+H2O+2Ag+3NH3↑.
点评 本题考查有机物的推断,难度中等,注意根据有机物的分子式、及性质进行推断,较好的考查学生的分析推理能力,是对有机化学知识的综合考查,是热点题型.


科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸和NaOH溶液反应,生成 l mol水时放热57.3 kJ | |
| B. | 含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ | |
| C. | 1L 0.l mol/L CH3COOH与1L 0.l mol/L NaOH溶液反应后放热为5.73 kJ | |
| D. | 1L 0.l mol/L HNO3与 1L 0.l mol/L NaOH溶液反应后放热为 5.73 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1.5 mol N2的体积约为33.6 L | |
| B. | NaOH的摩尔质量是40 g | |
| C. | 150mL 1 mol/LNaCl溶液与100mL 1 mol/LAlCl3溶液中的n(Cl-)相等 | |
| D. | 同温同压下,相同体积的C12和SO2气体所含的分子数一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
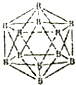 晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图).若其中有两个原子为10B,其余为11B,则该结构单元结构类型有( )
晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图).若其中有两个原子为10B,其余为11B,则该结构单元结构类型有( )| A. | 1种 | B. | 3种 | C. | 5种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com