
【题目】用括号中的试剂和方法除去各组物质中的少量杂质,正确的是( )
A.苯中的甲苯(酸化高锰酸钾溶液 分液)
B.乙醇中的水(无水硫酸铜 干燥)
C.乙醇中的乙酸(NaOH溶液 分液)
D.溴乙烷中的乙醇(水 分液)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铝热反应原理可以应用在生产上,例如焊接钢轨、冶炼难熔金属、制作传统的烟火剂等。某小组同学在研究铝热反应时,进行如下讨论和实验。
(1)关于铝热反应有以下两种认识,其中正确的是___________(填字母号)。
a .该反应需在高温下发生,所以该反应吸热
b.因为铝的还原性较强,所以铝能将相对不活泼的金属从其化合物中置换出来
(2)铝和氧化铁反应的化学方程式是______________________________________。
(3)铝和氧化铁反应所得固体成分的初步确定。
实验序号 | 操作及现象 |
i | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
ii | 向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色 |
①由上述实验可知:溶液中Fe元素的存在形式有______________________。
②i中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,可选用的试剂是_________________________________。
③ii中生成O2的化学方程式是______________________________。进一步的实验表明,上述固体样品中Fe元素的存在形式有Fe、Fe2O3、Fe3O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,选用了下图所示实验装置.
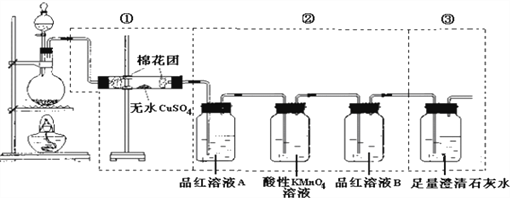
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式 ___________________________.
(2)①中无水硫酸铜的作用是__________________________.
(3)②中酸性KMnO4溶液的作用是______________________________.
(4)②中两次用到品红溶液,它们的作用分别是A______________,B________________________.
(5)①装置和②装置不能互换的原因_______________________________
(6)证明产物中有CO2的离子反应方程式_________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质①乙烷 ②乙炔 ③甲苯 ④苯 ⑤聚乙烯 ⑥对苯二酚 ⑦溴乙烷 ⑧葡萄糖,其中既能与溴水反应又能与酸性高锰酸钾溶液反应的是( )
A.②③④⑤⑧
B.②③④⑥⑦⑧
C.②⑥⑧
D.②⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
①非金属元素不可能组成离子化合物
②构成分子晶体的微粒一定含有共价键
③共价化合物中可能含有离子键
④离子化合物中可能含有共价键
⑤非极性键只存在于双原子单质分子里
⑥不同元素组成的多原子分子里的化学键一定都是极性键
A. ①②④⑥ B. ②④⑤⑥
C. ①③⑤⑥ D. 只有④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富铁铝土矿(主要含有A12O3、Fe2O3、FeO和SiO2)可制备新型净水剂液体聚合硫酸铝铁[AlaFeb(OH)m(SO4)n].研究发现,当a=b时净水效果最好.工艺流程如下(部分操作和产物略):![]()
(1)A12O3与H2SO4发生反应的离子方程式是 .
(2)测得滤液中 ![]() >1.加入FeSO47H2O和H2O2的作用是(结合化学用语说明) .
>1.加入FeSO47H2O和H2O2的作用是(结合化学用语说明) .
(3)将溶液A电解得到液体聚合硫酸铝铁.装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)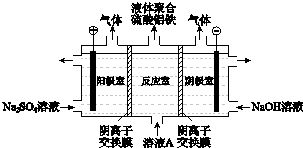
①阴极室的电极反应式是 .
②电解过程阳极室溶液pH的变化是(填“增大”、“减小”或“不变”).
③简述在反应室中生成液体聚合硫酸铝铁的原理 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分:

(1)根据元素周期律,请你预测,H3AsO4、H3PO4的酸性强弱:H3AsO4________H3PO4(填“>”、“<”或“=”).
(2)根据NaH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第________族.
(3)元素甲是第三周期金属元素中原子半径最小的元素,该元素的离子与过量氨水反应的离子方程式为:__________________________________________________________.
(4)周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用.已知R元素的原子有4个电子层,其最高价氧化物的分子式为RO3,则R元素的名称为 : _____________________________________.
(5)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构.用电子式表示羰基硫分子的形成过程:_____________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示(部分物质与条件已略去).已知A是由两种元素组成的黑色粉末,B由两种元素组成、其摩尔质量为65gmol﹣1 , C是空气中含量最多的单质,D是白色粉末且焰色反应呈黄色,E是一种紫红色金属,F是一种无色气体单质,H是一种红棕色气体,I是最常见的液体,K是一种强碱. 
(1)F的化学式为 .
(2)K的电子式为 .
(3)写出反应①的化学方程式:
(4)写出反应②的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置研究电化学原理,下列分析中错误的是( ) 
选项 | 连接 | 电极材料 | 分析 | |
a | b | |||
A | K1 K2 | 石墨 | 铁 | 模拟铁的吸氧腐蚀 |
B | K1 K2 | 锌 | 铁 | 模拟钢铁防护中牺牲阳极的阴极保护法 |
C | K1 K3 | 石墨 | 铁 | 模拟电解饱和食盐水 |
D | K1 K3 | 铁 | 石墨 | 模拟钢铁防护中外加电流的阴极保护法 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com