
| A���ɺ���ת��Ϊ���������ȷ�Ӧ���������ĺ��������Ȱ��� |
| B���ɺ���ת��Ϊ�����Ƿ��ȷ�Ӧ���������ĺ��������Ȱ��� |
| C���ɺ���ת��Ϊ�����Ƿ��ȷ�Ӧ���������ĺ��������Ȱ��� |
| D���ɺ���ת��Ϊ���������ȷ�Ӧ���������ĺ��������Ȱ��� |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
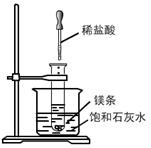
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����֪2H2(g)+O2(g) ==2H2O(l)����H=��571.6kJ��mol-1����H2��ȼ����Ϊ285.8kJ��mol-1 |
| B����֪4P�����ף�s��="=" P4�����ף�s������H>0������ױȺ����ȶ� |
| C����20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ����������ϡ�����ϡNaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ�� NaOH(aq)+CH3COOH(aq) ="=" CH3COONa(aq) + H2O(l) ��H =��57.4kJ��mol-1 |
| D����֪2C(s)+2O2(g)=2CO2(g) ��H1��2C(s)+O2(g)="2CO(g)" ��H2�����H1>��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ˮ�ֽ������������ | B��������� |
| C������������������������� | D��ϡ�����ϡ����������Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������������������۷ֱ���ȫȼ�գ�ǰ�߷ų������� |
B���ɡ�C��ʯī��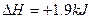 ��mol��1��֪���ʯ��ʯī�ȶ� ��mol��1��֪���ʯ��ʯī�ȶ� |
| C��ϡ��ǿ���ϡ��ǿ����Һ��Ӧ���Ȼ�ѧ����ʽ��Ϊ�� H����OH�� 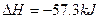 ��mol��1 ��mol��1 |
| D����25�桢101 kPaʱ��1��������ȫȼ������H2O�ų�����142.9kJ���� |
 O2��g����
O2��g����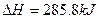 ��
�� mol��1
mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����������O2��O3�������ͣ���O2��O3Ϊ���ȷ�Ӧ |
| B����������O2��O3�������ߣ���O2��O3Ϊ���ȷ�Ӧ |
| C��O2��O3�ȶ���3O2(g)="=" 2O3(g)��H=��284.2 kJ/mol |
| D��O2��O3�ȶ���3O2(g)="=" 2O3(g)��H="+284.2" kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Һ̬ˮ���� | B������ȼ�� |
| C��Ũ�����ϡ�� | D��Ba��OH��2��8H2O��NH4Cl�����壩��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������¶ȣ�һ���ʹ����ӵİٷ������������Ӧ�������� |
| B�������֮�䷢������ײһ��Ϊ��Ч��ײ |
| C���ɱ�������һ�����У���S��0 |
D�����ڷ�Ӧ��CO (g)+H2O (g)  CO2 (g)+H2 (g)������ʱ���¶����ߣ�H2Ũ�������������Ӧ���ʱ�Ϊ��ֵ CO2 (g)+H2 (g)������ʱ���¶����ߣ�H2Ũ�������������Ӧ���ʱ�Ϊ��ֵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
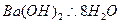 �������Ȼ�茶��巴Ӧ
�������Ȼ�茶��巴Ӧ�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com