
| A | B | C | D | |
| 强电解质 | AgCl | SO3 | 醋酸 | 熔融NaOH |
| 弱电解质 | 晶体桂 | BaSO4 | HF | Fe(OH)3 |
| 非电解质 | CH4 | 液氨 | C2H5OH | C02 |
| A. | A | B. | B | C. | C | D. | D |
分析 在水溶液中或熔融状态下能完全电离的化合物为强电解质,包括强酸、强碱、绝大多数盐和金属氧化物;
在水溶液中和熔融状态下均只能部分电离的化合物为弱电解质,包括弱酸、弱碱和水;
在水溶液中和熔融状态下均不能导电的化合物为非电解质,据此分析.
解答 解:A、晶体硅是单质,故不是电解质,更不是弱电解质,故A错误;
B、SO3在水溶液中导电和其本身无关,在熔融状态下不能导电,故为非电解质;BaSO4在熔融状态下能完全电离,故为强电解质,故B错误;
C、醋酸在水溶液中只能部分电离,故为弱电解质,故C错误;
D、NaOH在熔融状态能完全电离,故为强电解质;Fe(OH)3在水溶液中和熔融状态下只能部分电离,故为弱电解质;C02在水溶液中导电和其本身无关,在熔融状态下不能导电,故为非电解质,故D正确.
故选D.
点评 本题考查了电解质和非电解质以及强弱电解质的判断,难度不大,应注意的是电解质和非电解质必须为化合物.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
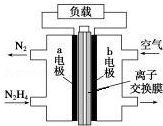 液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列 关于该电池的叙述错误的是( )
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列 关于该电池的叙述错误的是( )| A. | b 极发生还原反应 | |
| B. | a 极的反应式为 N2H4-4e-═N2↑+4H+ | |
| C. | 放电时,电流从 b 极经过负载流向 a 极 | |
| D. | 其中的离子交换膜需选用阴离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Cl-、NO3-、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | K+、SO42-、Cu2+、NO3- | D. | NH4+、OH-、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
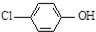 ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )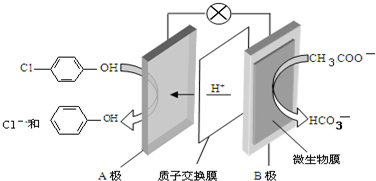
| A. | 当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.1NA | |
| B. | A极的电极反应式为 +e-=Cl-+ +e-=Cl-+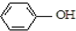 | |
| C. | 电流方向从B极沿导线经小灯泡流向A极 | |
| D. | B为电池的正极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2015年2月科学家成功观察到CO与O形成化学键生成C02的全过程(CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K).下列说法不正确的是( )
2015年2月科学家成功观察到CO与O形成化学键生成C02的全过程(CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K).下列说法不正确的是( )| A. | 该过程可以表示为:CO+O$\frac{\underline{\;催化剂\;}}{\;}$C02 | |
| B. | 该过程中有热量放出 | |
| C. | 催化剂能降低反应的活化能 | |
| D. | 钌催化剂能改变该反应的焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质 | B. | 混合物 | C. | 无机物 | D. | 有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCl2浓溶液 | B. | NaOH浓溶液 | C. | NH4Cl浓溶液 | D. | MgCl2浓溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com