
【题目】新康泰克能够缓解感冒时带来的鼻塞、流鼻涕和打喷嚏等症状,其有效成分为伪麻黄碱。伪麻黄碱D的一种合成路线如下:
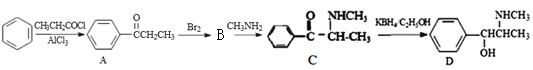
回答下列问题:
(1)苯的质谱图中最大的质荷比为___________,伪麻黄碱D的分子式为____________。
(2)写出由苯生成A的化学方程式:___________________________________________,其反应类型为_________________。
(3) B的结构简式为____________。
(4)满足下列要求的C的同分异构体有___________种;
①属于苯的一元取代物; ②含有-CONH-,且无-NH2 ;③不能发生银镜反应;其中苯环侧链的核磁共振氢谱有3组峰,且峰面积之比为6:1:1的一种有机物的结构简式为_________________。
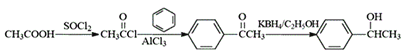
(5)已知:![]() 参照上述合成路线,设计一条由苯和乙酸为起始原料制备的合成
参照上述合成路线,设计一条由苯和乙酸为起始原料制备的合成 路线:____________________________________。
路线:____________________________________。
【答案】78 C10H15NO ![]()
![]() CH3CH2COCl
CH3CH2COCl![]()
![]()
![]() HCl 取代反应
HCl 取代反应 ![]() 10
10  或
或 ![]()
【解析】
(1)苯的最大的质荷比为就是其相对分子质量;观察D的结构简式写出D的分子式;
(2)苯和CH3CH2COCl发生取代反应生成![]() 和HCl;
和HCl;
(3)依据C的结构简式分析可知,溴和A发生取代反应及取代氢原子的位置;
(4)满足①属于苯的一元取代物,要求苯环上只能有一个氢被取代,②含有-CONH-,且无-NH2,要求含有肽键,但无-NH2,③不能发生银镜反应,要求不能含有醛基,并写出苯环的侧链上只能含有三种氢原子,氢原子个数比为6:1:1,按要求书写其同分异构体;
(5)由题意可知,合成路线是乙酸先发生已知条件中给出的反应,再与苯发生取代反应,最后再进行还原反应即可:
(1)苯的最大的质荷比就是其相对分子质量,苯的相对分子质量为78,所以苯的最大的质荷比为78;通过观察D的结构简式可知D的分子式为:C10H15NO;
本题答案为:78,C10H15NO。
(2)苯和CH3CH2COCl发生取代反应生成![]() 和HCl,反应的化学方程式为:
和HCl,反应的化学方程式为:![]()
![]() CH3CH2COCl
CH3CH2COCl![]()
![]()
![]() HCl;
HCl;
本题答案为:![]()
![]() CH3CH2COCl
CH3CH2COCl![]()
![]()
![]() HCl、取代反应。
HCl、取代反应。
(3)通过C的结构简式分析可知,溴和A发生取代反应及溴取代氢原子的位置,B的分子式应为:![]() ;
;
本题答案为:![]() 。
。
(4)满足①属于苯的一元取代物,要求苯环上只能有一个氢被代,②含有-CONH-,且无-NH2,要求含有肽键,但无-NH2,③不能发生银镜反应,要求不能含有醛基,符合条件的![]() 的同分异构体的侧链为:—CONHCH2CH2CH3、—CONHCH(CH3)2、—CH2CONHCH2CH3、—CH2CH2CONHCH3、—CH(CH3)CONHCH3、—NHOCCH2CH2CH3、—NHOCCH(CH3)2、—CH2NHOCCH2CH3、—CH2CH2NHOCCH3、—CH(CH3)NHOCCH3,共10种,其中苯环的侧链上只能含有三种氢原子,氢原子个数比为6:1:1,有机物的结构简式为:
的同分异构体的侧链为:—CONHCH2CH2CH3、—CONHCH(CH3)2、—CH2CONHCH2CH3、—CH2CH2CONHCH3、—CH(CH3)CONHCH3、—NHOCCH2CH2CH3、—NHOCCH(CH3)2、—CH2NHOCCH2CH3、—CH2CH2NHOCCH3、—CH(CH3)NHOCCH3,共10种,其中苯环的侧链上只能含有三种氢原子,氢原子个数比为6:1:1,有机物的结构简式为: 或
或![]() ;
;
(5)由题意可知,合成路线是乙酸先发生已知条件中给出的反应,再与苯发生取代反应,最后再进行还原反应即可:
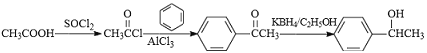 ;
;
本题答案为: 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氨和硝酸都是重要的工业原料。
(1)标准状况下,将500 L氨气溶于水形成1 L氨水,则此氨水的物质的量浓度为__mol· L-1(保留三位有效数字)。工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为__。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为__。
下列反应中的氨与氨氧化法中的氨作用相同的是__。
A.2Na+2NH3===2NaNH2+H2↑ B.2NH3+3CuO===3Cu+N2+3H2O
C.4NH3+6NO===5N2+6H2O D.HNO3+NH3===NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH﹣===NO2-+NO3-+H2O和NO+NO2+2OH﹣===□ +H2O(配平该方程式)。______________
(3)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀HNO3500 mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1 L 1 mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2 g。
①Cu与稀HNO3反应的离子方程式为__。
②Cu与Cu2O 的物质的量之比为__。
③HNO3的物质的量浓度为__mol·L-1。
(4)有H2SO4和HNO3的混合溶液20 mL,加入0.25 molL﹣1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为__mol·L-1,HNO3的物质的量浓度为__mol·L-1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠的化合物用途广泛,回答下列问题:
(1)多硫化钠(Na2Sx)用作聚合的终止剂。钠原子价层电子的轨道表达式(电子排布图)为___________,基态S原子电子占据最高能级的电子云轮廓图为___________,其中Na2S4中存在的化学键有:___________。
A.离子键 B.极性共价键 C.π键 D.非极性共价键
(2)r(S2-)>r(Na+)的原因是___________。
(3)Na2SO3常用作工业的脱氧剂和漂白剂,其阴离子的中心原子的杂化形式是___________,空间构型是______________________。
(4)下表列出了钠的卤化物的熔点:
化学式 | NaF | NaCl | NaBr | NaI |
熔点/℃ | 995 | 801 | 775 | 651 |
①NaF的熔点比NaI的熔点高的原因是_________________________________;
②NaCl晶格能是786 kJ/mol,则NaF的晶格能可能是___________。
A. 704 kJ/mol B. 747kJ/mol C 928 kJ/mol
(5)NaH具有NaCl型的立方晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,则H-的半径为___________pm;NaH的理论密度是___________g·cm-3(保留三位有效数字)。[H—1、Na—23]
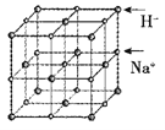
(6)首例被发现的带结晶水的超导材料晶体化学式为Na0.35CoOx·1.3H2O,具有……-CoO2-H2O-Na-H2O-CoO2-H2O-Na-H2O-……层状结构,已知CoOx层的构型部分如图,其中粗线画出的是其二维晶跑,则x=___________。
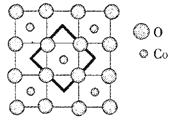
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酒厂生产的一种白酒醇香浓厚,其标签上标有“55°”的字样,它表示( )
A.该酒是在温度为55℃的条件下酿造的
B.喝了该酒后,人体温度可达到55℃
C.该酒的沸点为55℃
D.该酒中乙醇的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。

已知:在溶液中,FeSO4+NO![]() [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列对该实验相关描述错误的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列对该实验相关描述错误的是
A. 装置F、I中的试剂依次为水,硫酸亚铁溶液
B. 装置J收集的气体中不含NO
C. 实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D. 若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是 ( )


A. 由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的ΔH<0
B. 由图Ⅱ知,反应在t6时刻,NH3体积分数最小
C. 由图Ⅱ知,t3时采取增大反应体系压强的措施
D. 图Ⅲ表示在10 L容器、850℃时的反应,由图知,到4 min时,反应放出51.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在装有MnO2的试管中加入H2O2可以快速制取O2,回答下列问题:
(1)H2O2中O的化合价是_____,写出H2O2中含有的化学键类型____(填字母序号)。
A.极性共价键 B.非极性共价键 C.离子键
(2)写出该反应的化学方程式 _______。
(3)MnO2的作用是______。
(4)下列措施可以加快该化学反应速率的是_______。
A.滴加FeCl3溶液 B.加热 C.降低压强 D.增大H2O2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备 Fe(OH)2,装置如右图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是
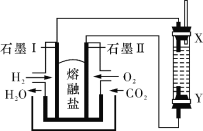
A. 石墨电极Ⅱ处的电极反应式为O2+4e-=2O2-
B. X是铁电极
C. 电解池中有1mol Fe溶解,石墨Ⅰ耗H2 22.4 L
D. 若将电池两极所通气体互换,X、Y两极材料也互换, 实验方案更合理。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com