
| A.Fe3+、K+、Cl-、MnO4- | B.K+、Na+、NO3-、Cl- |
| C.Zn2+、Al3+、SO42-、Cl- | D.Ba2+、NH4+、Cl-、HCO3- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
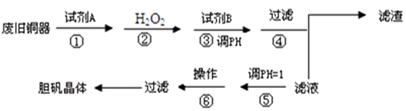
| 物质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在碱性溶液中 Na+、K+、ClO-、S2- |
| B.在pH=13的溶液中 Al3+、Na+、SO42-、Cl- |
| C.在水电离出的氢离子浓度为1×10-13的溶液中 Na+、NH4+、AlO2-、CO32- |
| D.在酸性溶液中 Na+、K+、MnO4-、NO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu2+、H+、Cl- | B.K+、Cl-、CO32- |
| C.K+、OH-、CO32- | D.K+、H+、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Ba2+和NO3- | B.Na+和Cl- | C.Na+和NO3- | D.Ag+和SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.MgCO3与盐酸反应:CO32-+2H+ ="=" CO2↑+H2O |
| B.Mg(OH)2与H2SO4反应:Mg2++2OH-+2H++SO42- ="=" MgSO4↓+2H2O |
| C.镁与醋酸反应:Mg+2H+ ="=" Mg2++H2↑ |
| D.工业上以海水为原料制备Mg(OH)2:Ca(OH)2+Mg2+ ="=" Mg(OH)2↓+Ca2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.PH=0的溶液:K+、Ca2+、HCO3-、NO3- |
| B. c(H+水)=1×10-10 mol/L溶液中:K+、Fe2+、SO42-、NO3- |
| C.使紫色石蕊变蓝的溶液:K+、Na+、CH3COO-、SO42- |
| D.存在较多的Na+、SO42-、OH-的溶液中:Mg2+、Ba2+、Br- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com