
烧碱和氯气都是重要的基本化工原料,它们大多来自氯碱工业,氯碱工业的工艺流程如下图所示:
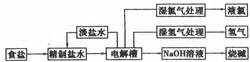
(1)电解饱和食盐水的总反应方程式为______,阳极发生的电极反应为_______。
(2)工业生产用的食盐水进入电解槽之前需精制,请简要说明需要精制的原因。
(3)目前氯碱工业主要采用的方法有三种,它们各有特点(见表)。
| 方法 | 电解槽特点 | 产品中氯 化钠含量 | 电解液中氢 氧化钠含量 | 总能耗 (kW.h?t-1) | 其他 |
| 隔膜法 | 使用石棉纤维制成的隔膜隔开阴阳极 | 较大 | 低 | 高 | 细微石棉吸入人的肺内有损健康,目前正被离子膜交换法取代 |
| 汞法 | 由独立的电解室和解汞室构成,氯气和氢气在不同的室产生 | 低 | 很高 | 高 | 汞易对环境造成污染,在我国已经被淘汰 |
| 离子交换膜法 | 使用能选择性通过离子的离子膜替代隔膜法中石棉隔膜 | 很低 | 较高 | 低 | 占地少、生产能力大、能连续生产,是氯碱工业的发展方向 |
请比较三种方法的优缺点,指出哪些方面的主要因素不断促进着电解槽革新。
(4)氯碱化工厂的选址比较特殊,如通常不会单独建氯碱化工厂,而是与农药厂、有机化工、制药厂、盐酸厂等建在一起,请分析这种建厂方式的原因和所带来的好处
科目:高中化学 来源: 题型:
| A、Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒 | B、自行车钢架生锈主要是电化学腐蚀所致 | C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 | D、燃煤时加入适量石灰石,可减少废气中SO2的量 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东广州六中高一上学期期末考试化学试卷(带解析) 题型:填空题
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl-、Br-(溴离子)、SO42-、Na+、Mg2+、Ca2+等,都是重要资源。
(1)写出步骤①、②、④分离提纯的方法:
① ② ④
(2)步骤②分离提纯过程中需要选用主要玻璃仪器的名称 。
(3)欲除去初步提纯后的粗盐中的MgCl2、CaCl2和Na2SO4,应向该粗食盐水中依次加入NaOH溶液、 溶液、 溶液,然后过滤;为尽可能除去杂质,每次加入的试剂应 。向所得溶液中滴加 至无气泡产生,再经蒸发结晶得到食盐晶体。
(4)检验淡水中是否含有Cl-的操作现象及结论 。
(5)写出加入试剂a后,发生反应的离子方程式 、
(6)工业上用电解饱和食盐水的方法生产氯气、氢气和烧碱,请写出利用氯气和消石灰制取漂白粉的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届广东广州六中高一上学期期末考试化学试卷(解析版) 题型:填空题
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl-、Br-(溴离子)、SO42-、Na+、Mg2+、Ca2+等,都是重要资源。
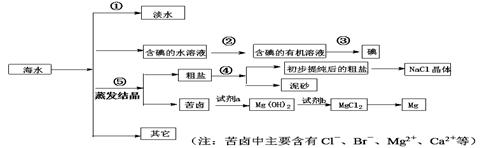
(1)写出步骤①、②、④分离提纯的方法:
① ② ④
(2)步骤②分离提纯过程中需要选用主要玻璃仪器的名称 。
(3)欲除去初步提纯后的粗盐中的MgCl2、CaCl2和Na2SO4,应向该粗食盐水中依次加入NaOH溶液、 溶液、 溶液,然后过滤;为尽可能除去杂质,每次加入的试剂应 。向所得溶液中滴加 至无气泡产生,再经蒸发结晶得到食盐晶体。
(4)检验淡水中是否含有Cl-的操作现象及结论 。
(5)写出加入试剂a后,发生反应的离子方程式 、
(6)工业上用电解饱和食盐水的方法生产氯气、氢气和烧碱,请写出利用氯气和消石灰制取漂白粉的化学方程式 。
18.
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl-、Br-(溴离子)、SO42-、Na+、Mg2+、Ca2+等,都是重要资源。

(1)写出步骤①、②、④分离提纯的方法:
① ② ④
(2)步骤②分离提纯过程中需要选用主要玻璃仪器的名称 。
(3)欲除去初步提纯后的粗盐中的MgCl2、CaCl2和Na2SO4,应向该粗食盐水中依次
加入NaOH溶液、 溶液、 溶液,然后过滤;为尽可能除去杂质,每次加入的试剂应 。向所得溶液中滴加 至无气泡产生,再经蒸发结晶得到食盐晶体。
(4)检验淡水中是否含有Cl-的操作现象及结论 。
(5)写出加入试剂a后,发生反应的离子方程式 。
(6)工业上用电解饱和食盐水的方法生产氯气、氢气和烧碱,请写出利用氯气和石灰
乳制取漂白粉的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com