
常温下,下列叙述正确的是:
A.K2CO3溶液中,1/2c(K+)=c(CO32-)+c(HCO3-)+c(H2CO3)
B.某浓度的NaAc溶液的pH=8,则该溶液中的c(Na+)-c(Ac-)=9.9×10-7mol/L
C.物质的量浓度相等的①NH4Cl、②(NH4)2SO4两种溶液,c(NH4+)大小顺序为:①>②
D.10mLpH=12的烧碱溶液中加入pH=2的酸HA至中性,所需酸溶液的体积V≥10mL
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.碳原子数≤10 的烷烃,其一氯代物没有同分异构体的烷烃共有3种
B.烯烃、炔烃、芳香烃都能与溴水反应而使其褪色
C.等质量的CH≡CH和C6H6完全燃烧时消耗等物质的量的氧气
D.分子式为C6H12与C3H6的两种烃一定互为同系物
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
2015年诺贝尔生理学或医学奖授予中国药学家屠呦呦以及爱尔兰科学家威廉·坎贝尔和日本科学家大村智,表彰他们在寄生虫疾病治疗研究方面取得的成就。屠呦呦先驱性地发现了青蒿素,开创了疟疾治疗新方法。右图为青蒿素,关于该物质的下列说法正确的是
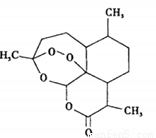
A.青蒿素化学式为C15H20O5
B.在光照条件下可能发生取代反应
C.可以与氢气发生加成反应
D.水浸青蒿对治疗疟疾有良好的疗效
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:填空题
已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小。请回答:
(1)A、B、C、D的第一电离能由小到大的顺序是__________(用元素符号填空)
(2)化合物BD3的分子构型为__________,B的原子轨道杂化类型为__________。B元素氢化物的沸点低于其同族上周期元素的氢化物的原因是__________。
(3)己知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物.则F的基态原子价电子排布式为__________,CN-与__________(一种分子)互为等电子体.消除CN-剧毒性的方法之一是加入浓的双氧水,可将其转化为可溶性碳酸盐及氨气,写出该反应的离子方程式:__________。
(4)①E基态原子的价电子排布为__________,②EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为__________。
③已知该晶体的摩尔质量为M(g/mol),其中E4+的氧配位数为__________。若该晶胞边长为anm,可计算该晶体的密度为__________g/cm3(阿伏加德罗常数为NA)。

查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:填空题
(1)在298K,100kPa时.CH4的燃烧热是890.0kJ/mol,写出该反应的热化学方程式__________。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,共放出QkJ热量(假定热量未损失),则CH4和CO的物质的量的比为__________。
(2)利用甲烷的燃烧反应设计一个燃料电池,用氢氧化钾溶液作电解质溶液.多孔石墨作电极,在电极上分别通入甲烷和氧气,通入甲烷气体的电极上发生的电极反应是___________,当电路中转移12mol电子时,实际提供的电能是890.0kJ,则该电池的能量转化效率是__________。
(3)将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中形成如图装置:

①当开关K1闭合,则铁发生电化学腐蚀中的__________腐蚀。
②当开关K2闭合,则总反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:选择题
硒(34Se)元素是人体必需的微量元素,它在自然界有六种核素。下列有关78Se和80Se的说法不正确的是
A.两者的质量数不同
B.两者的中子数不同
C.两者的核外电子数相同
D.两者互为同素异形体
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。化合物有E最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯.玉米淀粉等发酵制得,E的钙盐是人们喜爱的补钙剂之一。

已知: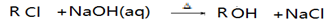
(1)D中所含官能团名称。E→G的反应类型为_________。
(2)聚合物F的结构简式。聚合物G的结构简式_________
(3)在一定条件下,两分子E在浓硫酸作用下形成一种六元环状化合物,该化合物的结构简式是_________。
(4)B转化为C的化学反应方程式是_________。
(5)下列四种化合物与E互为同分异构体的是_________。
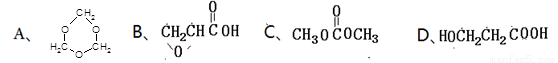
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中文科化学试卷(解析版) 题型:选择题
实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是
A.加水稀释 B.加少量NaOH溶液
C.降低温度 D.锌片改为锌粒
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南师大附中高一下期中化学试卷(解析版) 题型:选择题
PH3一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低。下列判断错误的是
A.PH3分子中存在极性共价键
B.P—H键键长比N—H键键长长
C.PH3沸点低于NH3沸点,因为P-H键键能低
D.PH3分子稳定性低于NH3分子,因为N-H键键能高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com