
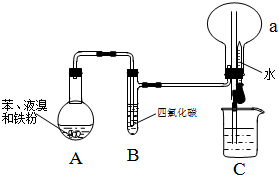
 某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应.
某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应. .
.分析 (1)苯与液溴在铁做催化剂条件下反应生成溴苯和溴化氢;
(2)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象,即可证明发生取代反应,若发生加成反应,则不会生成溴化氢,不会产生喷泉;
(3)由于反应放热,苯和液溴均易挥发,溴的存在干扰检验H+和Br-;
(4)溴与氢氧化钠反应生成易溶于水的溴化钠,溴苯不溶于水,据此选择分离方法.
解答 解:(1)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,苯分子里的氢原子被溴原子所代替,方程式为 ;
;
故答案为: ;
;
(2)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象,即可证明发生取代反应,若发生加成反应,则不会生成溴化氢,不会产生喷泉;
故答案为:a中发生喷泉现象;
(3)由于反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防干扰检验H+和Br-,
故答案为:除去未反应的苯蒸气和溴蒸气;
(4)溴苯中混有的少量溴,常向混合物中加入的试剂是氢氧化钠,化学式为NaOH,溴与氢氧化钠反应生成溶于水的溴化钠,溴苯不溶于水,产生分层,可以用分液漏斗分离;
故答案为:NaOH;分液.
点评 本题考查有机物的性质实验,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握苯与溴发生取代反应的特点,把握实验的原理和操作方法,难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 该烃分子中至少有5个碳原子处于同一直线上 | |
| B. | 该烃分子中所有碳原子可以处于同一平面上 | |
| C. | 该烃分子中至少有12个碳原子处于同一平面上 | |
| D. | 1 mol该烃能与8 mol氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
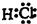 ;反应③中被破坏的化学键属于非极性键(填“极性”或“非极性”).
;反应③中被破坏的化学键属于非极性键(填“极性”或“非极性”).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
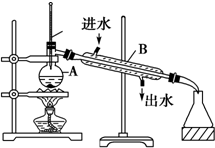 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题| 物质 | 熔点/℃ | 沸点/℃ | 密度 /g•cm-3 | 溶解性 |
| 乙二醇 (C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水 和乙醇 |
| 丙三醇 (C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
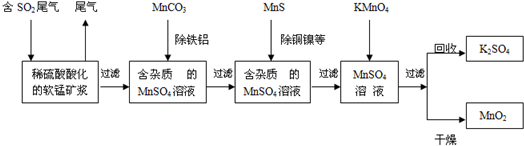
 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:学习小组的同学设计了滴定的方法测定x值.
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:学习小组的同学设计了滴定的方法测定x值.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com