
A.Cl2+2Br-====Br2+2Cl-
B.Fe2++2Br-+Cl2====Fe3++Br2+2Cl-
C.2Fe2++2Br-+2Cl2====2Fe3++4Cl-+Br2
D.2Fe2++4Br-+3Cl2====2Fe3++6Cl-+2Br2
科目:高中化学 来源: 题型:
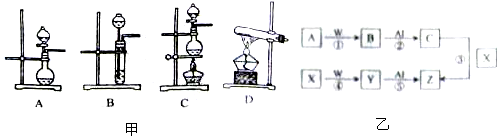
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制氧气 | H2O2→O2 | |
| ② | 制氨气 | NH4Cl→NH3 | |
| ③ | 制氯气 | HCl→Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Fe2+和Cl2在溶液中因发生氧化还原反应而不能大量共存。现将过量的Cl2通入FeBr2溶液中,下列离子方程式正确的是( )
A.Cl2+2Br-====Br2+2Cl- B.Fe2++2Br-+Cl2====Fe3++Br2+2Cl-
C.2Fe2++2Br-+2Cl2====2Fe3++4Cl-+Br2 D.2Fe2++4Br-+3Cl2====2Fe3++6Cl-+2Br2
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(8分)阅读下列材料后,回答相应问题。
一个体重50Kg的健康人大约含铁2g,这2g铁在人体中不是以单质金属形式存在,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
(1)人体中经常进行的相互转化,在A过程中,Fe2+做 剂,在B过程中,Fe3+做 剂。
(2)“服用维生素C,可使食物中三价铁离子还原成二价铁离子。”这句话指出,维生素C在这一反应中做 _剂,具有 性。
(3)已知:氧化性Cl2 > Br2 > Fe3+,还原性Fe2+ >Br- >Cl-,则向0.2mol/L 1LFeBr2溶液中通入标准状况下氯气2.24L,被氧化的粒子是 ,此反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2012届福建省高二下学期第一学段考试化学试卷 题型:填空题
(6分) 氢氧化铜悬浊液中存在如下平衡:
Cu(OH)2 (s)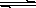 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于 。
(2)除去CuCl2溶液中少量的Fe2+,可以按照下面的流程进行:
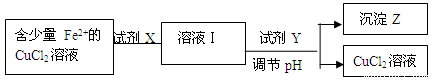
已知Fe2+ 、Cu2+ 、Fe3+ 三种离子开始沉淀和完全沉淀时溶液pH值如下:
|
金属 离子 |
pH |
|
|
开始沉淀 |
完全沉淀 |
|
|
Fe2+ |
7.6 |
9.6 |
|
Cu2+ |
4.4 |
6.4 |
|
Fe3+ |
2.7 |
3.7 |
①下列物质中适合作为试剂X的是
A.H2O2 B.KMnO4 C.HNO3 D.Cl2
②加入的Y及调节的pH范围是
A.CuCO3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com