
常温下,下列溶液中各微粒浓度关系或pH判定不正确的是
A.将5 mL 0.02 mol/L的H2SO4溶液与5 mL 0.02 mol/L NaOH溶液充分混合,若混合后溶液的体积为10 mL,则混合液的pH=2
B.某物质的溶液中由水电离的c(H+) = 1×10-a mol/L,若a>7,则pH一定为14-a
C.pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:①>③>②
D.CH3COONa溶液中加入少量KNO3固体后的碱性溶液一定有:
c(Na+) + c(H+) = c(CH3COO-) + c(OH-)
B
【解析】
试题分析:A、反应中硫酸是过量的,所以反应后溶液中c(H+)=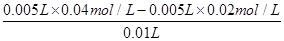 =0.01mol/L,则pH=2,A正确;
=0.01mol/L,则pH=2,A正确;
B、某物质的溶液中由水电离的c(H+)=1×10-a mol/L,若a>7,这说明该溶液中水的电离平衡是被破坏的。因此溶液可能显酸性,也可能显碱性,则pH不一定为14-a,也可能是a,B不正确;
C、酸性强弱顺序是醋酸>碳酸>苯酚,酸性越弱,相应的钠盐越容易水解,pH越大。因此pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:①>③>②,C正确;
D、根据电荷守恒可知,c(Na+) + c(H+)+c(K+) = c(CH3COO-) + c(OH-)+ c(NO3-)。由于c(K+) = c(NO3-),所以c(Na+) + c(H+) = c(CH3COO-) + c(OH-),D正确,答案选B。
考点:考查溶液中pH值计算、离子浓度大小比较等


科目:高中化学 来源:2012-2013学年四川省达州市高三第一次诊断性考试理综化学试卷(解析版) 题型:选择题
常温下,下列溶液中各微粒浓度关系不正确的是( )
A、PH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,C(Na+)大小关系:①>③>②
B、向氨水中滴加稀硫酸至溶液呈中性:C(NH4+)>C(SO42-)>C(OH-)=C(H+)
C、向1L 0.1mol/L的NaOH溶液中通入6.6gCO2:2C(Na+)=3[C(CO32-)+C(HCO3-)+C(H2CO3)]
D、 CH3COONa溶液中加入少量KNO3后的碱性溶液一定有:C(Na+)+C(H+)=C(CH3COO-)+C(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com