
【题目】下列各物质的晶体中,晶体类型相同的是( )
A.CCl4和NaCl
B.NaI和I2
C.CO2和C60
D.Mg和H2
科目:高中化学 来源: 题型:
【题目】已知,I2(aq)+I﹣(aq)![]() I3﹣(aq).某I2、KI溶液中,c(I3﹣)与温度(T)的关系如图所示(曲上任何一点都表示平衡状态).下列说法正确的是
I3﹣(aq).某I2、KI溶液中,c(I3﹣)与温度(T)的关系如图所示(曲上任何一点都表示平衡状态).下列说法正确的是
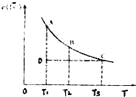
A. 反应I2(aq)+I﹣(aq)![]() I3﹣(aq)△H>0
I3﹣(aq)△H>0
B. 状态A的c (I2)比状态D的小
C. A点对应的反应速率大于C点对应的反应速率
D. 其他条件不变,向溶液中加入KI固体,平衡由C点移动到D点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用下列实验探究金属铝与铜盐溶液反应:下列说法正确的是( )
A. 由实验1 可以得出结论:金属铝的活泼性弱于金属铜
B. 实验2 中生成红色物质的离子方程式:Al+Cu2+═Al3++Cu
C. 溶液中阴离子种类不同是导致实验1、2 出现不同现象的原因
D. 由上述实验可推知:用砂纸打磨后的铝片分别与浓度均为0.2molL﹣1的盐酸和硫酸反应,后者更剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写不正确的是( )
A. H2SO4=2H++SO42- B. NaHCO3=Na++H++CO32-
C. FeCl3=Fe3++3Cl- D. Ba(OH)2=Ba2++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl—,消耗等物质的量浓度的AgNO3溶液的体积比为3:2:1,则上述溶液的体积比为( )
A. 1:1:1 B. 3:2:1
C. 6:3:2 D. 9:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g)ΔH 1=+489.0 kJ·mol-1,
C(s)+CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式: 。
(3)一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
①CO的平衡转化率(α)与温度、压强的关系如下图所示。

B、C两点的平衡常数K(B) K(C)(填“>”、“=”或“<”).
②某温度下,将2.0molCO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,CO的转化率= ,此温度下的平衡常数K= (保留二位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示.
CH3﹣CH═CH﹣CH3可简写为![]() .
.
(1)有机物X的键线式为: ,该有机物与H2加成时最多能消耗氢气的物质的量 ,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式 ,将Y加入酸性高锰酸钾溶液中的现象 .
,该有机物与H2加成时最多能消耗氢气的物质的量 ,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式 ,将Y加入酸性高锰酸钾溶液中的现象 .
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式: .
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO47H2O)是治疗缺铁性贫血药品的重要成分.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:

查询资料,得有关物质的数据如下表:
25℃时 | pH值 |
饱和H2S溶液 | 3.9 |
SnS沉淀完全 | 1.6 |
FeS开始沉淀 | 3.0 |
FeS沉淀完全 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,可选用的试剂为__________.
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是__________;在溶液中用硫酸酸化至pH=2的目的是:__________.
(3)操作IV的顺序依次为__________、冷却结晶、__________.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;
②____ __________________.
(5)测定绿矾产品中Fe2+含量的方法:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
(滴定时发生反应的离子方程式为:5Fe2++MnO4+8H+→5Fe3++Mn2++4H2O)。
①滴定时盛放KMnO4溶液的仪器为 (填仪器名称)
②判断此滴定实验达到终点的方法是 。
③写出酸性高锰酸钾滴定Fe2+的离子反应方程式: 。
④计算上述样品中FeSO4·7H2O的质量分数为 (结果保留3位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com