
| A������ˮ�м���NaOH��Һ�����ԣ�������Һ��c��Na+��=c��Cl-��+c��ClO-�� |
| B��Na2O2�ڿ����г��ڷ��ã����ձ�ΪNaHCO3��ĩ |
| C��ij��Һ�м��������ܲ�������������Һ�п��ܴ������ڣ�H+��SO42-��NO3-��Na+ |
| D���ڷ�ӦO3+2KI+H2O�T2KOH+I2+O2�У�ÿ����32gO2��ת�Ƶ�����ĿΪNA |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?����ģ�⣩����������ȼ��ʱ�õ�һ�ּص������ᄃ�壬��ṹ��ͼ��ʾ�������й�˵����ȷ���ǣ�������
��2012?����ģ�⣩����������ȼ��ʱ�õ�һ�ּص������ᄃ�壬��ṹ��ͼ��ʾ�������й�˵����ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
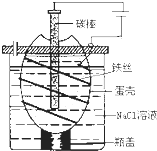 ��ҵ��ͨ����ⱥ���Ȼ�����Һ�ķ�������������ƺ�������ͼΪijʵ��С�����Ƶĵ�ⱥ��ʳ��ˮ�ļ���װ�ã�
��ҵ��ͨ����ⱥ���Ȼ�����Һ�ķ�������������ƺ�������ͼΪijʵ��С�����Ƶĵ�ⱥ��ʳ��ˮ�ļ���װ�ã�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
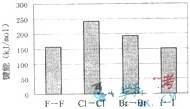 ��2009?�Ϻ�����������Դ�ı��⣬�̲��ŷḻ�Ļ�ѧԪ�أ����ȡ��塢��ȣ�
��2009?�Ϻ�����������Դ�ı��⣬�̲��ŷḻ�Ļ�ѧԪ�أ����ȡ��塢��ȣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com