
【题目】向体积均为2 L的两个恒容密闭容器中分别充入1molSiHCl3,维持容器的温度分别为T1℃和T2℃不变,发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
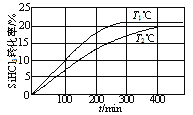
A.T1>T2
B.T1℃时,0~100min反应的平均速率v(SiHCl3)=0.001mol·(L·min)-1
C.T2℃时,反应的平衡常数:K=1/64
D.T2℃时,使用合适的催化剂,可使SiHCl3的平衡转化率与T1℃时相同
【答案】AC
【解析】
A. “先拐先平数值大”,升高温度,化学反应速率会增大,达到平衡的时间会缩短,图中可看出T1>T2,A项正确;
B. T1℃时,0~100min SiHCl3的转化率为10%,反应的平均速率v(SiHCl3)=![]() =0.0005mol·(L·min)-1,B项错误;
=0.0005mol·(L·min)-1,B项错误;
C. 从图中信息可以看出,T2℃时达到平衡SiHCl3的转化率为20%,则:
2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)
SiH2Cl2(g)+SiCl4(g)
起始量(mol/L) 0.5 0 0
转化量(mol/L) 0.1 0.05 0.05
平衡量(mol/L) 0.4 0.05 0.05,
则平衡常数K=![]() =1/64,C项正确;
=1/64,C项正确;
D. 催化剂不会使平衡移动,不会改变SiHCl3的平衡转化率,D项错误;
答案选AC。


科目:高中化学 来源: 题型:
【题目】2015年10月,中国科学家屠呦呦因为创制了新型抗疟药﹣﹣青蒿素,获得诺贝尔生理学或医学奖.青蒿素可由香茅醛为原料制取,下列说法不正确的是( )
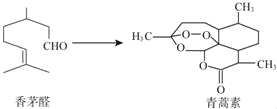
A.香茅醛能使Br2的CCl4溶液褪色
B.青蒿素分子式为C15H22O5
C.青蒿素在一定条件下可发生水解反应
D.二者均可与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3+5O2![]() 4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均反应速率v(X)为
4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均反应速率v(X)为
A. v(NH3)= 0.004molL-1s-1B. v(O2)= 0.15molL-1min-1
C. v(NO)= 0.008molL-1s-1D. v(H2O)= 0.16molL-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)==2C(g)+D(g),经2min后B的浓度减少0.6mol·L-1,下列说法正确的是
A. 用A表示的反应速率是0.4mol·L-1·min-1
B. 在2min末的反应速率,用B表示是0.3 mol·L-1·min-1
C. 分别用B、C、D表示反应的速率,其比值是3:2:1
D. 在这2min内B和C两物质浓度是逐渐减小的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种主族元素X、Y、Z、M和N在周期表中的位置如图所示。下列说法正确的是

A. M的原子半径比N小
B. Y和Z既可形成Z2Y,也可形成Z2Y2
C. X2M的热稳定性比X2Y强
D. M和N的氧化物的水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是
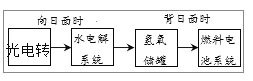
A.该能量转化系统中的水也是可以循环的
B.燃料电池放电时的负极电极反应式:2H2+4OH--4e-=4H2O
C.燃料电池放电时的正极电极反应式:2H2O+O2+4e-=4OH-
D.燃料电池系统产生的能量实际上来自于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在1L的密闭容器中充入NO2发生如下反应:2NO2(g)![]() N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
(1)该反应的ΔS__________0(填“>”、“<”或“=”)。
(2)当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01 mol·L-1,则NO2的平衡转化率(α)是_____________。25℃时上述反应的平衡常数K =_________。
(3)25℃时,实验测得该反应的活化能Ea=92.4 kJ·mol-1。下列能量关系图合理的是_____。
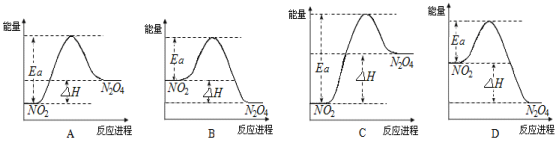
(4)如把该密闭容器放入80℃的热水中,则气体的颜色___________(填“不变”、“加深”或“变浅”),NO2的转化率___________(填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、硫、碳的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:
(1)根据A对应的化合价和物质类别,A为___________(写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有____________。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________,反应的离子方程式为______________。
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:_______________。
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为_____。
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式_______。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com