
【题目】将5mL10mol/L的硫酸稀释到100mL,得硫酸溶液的物质的量浓度是( )
A. 0.2mol/LB. 0.5mol/LC. 2mol/LD. 5mol/L
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol/L的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却。
其正确的操作顺序为___________ ⑤⑥⑤__________。本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、胶头滴管、还有_____________________。
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为_________ g。要完成本实验该同学应称出_________ g NaOH。

(3)对所配制的NaOH溶液进行测定,发现其浓度低于1.0mol/L。在溶液配制过程中,下列操作会引起该误差的有_________(填序号)。
A.转移溶解的溶液后没有洗涤烧杯和玻璃棒
B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶未干燥就用来配制溶液
D.称量NaOH固体时动作太慢,耗时太长
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
F.定容时仰视刻度线
G.NaOH固体溶解后未经冷却即转移到容量瓶中
(4)氢氧化钠是一种用途十分广泛的重要化工原料,工业上主要通过电解氯化钠饱和溶液的方法![]() 。试用单线桥法标出该反应中电子转移的方向和数目____________________。实验测得,反应中生成的气体在标准状况下的体积为4.48L,则耗氧化剂的物质的量为_________mol。
。试用单线桥法标出该反应中电子转移的方向和数目____________________。实验测得,反应中生成的气体在标准状况下的体积为4.48L,则耗氧化剂的物质的量为_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种金属的合金13 g,与足量稀硫酸反应后,在标准状况下产生气体11.2 L,则组成该合金的金属不可能是( )
A.Mg和Al
B.Mg和Zn
C.Al和Zn
D.Al和Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学,化学实验在学习中具有重要的作用。下列关于实验的叙述中正确的有 ____________。
A.不慎碰翻燃着的酒精灯失火,应立即用湿布灭火
B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH清洗
C.用托盘天平称量物品质量时,物品应置于右盘
D.实验时应节约药品,实验剩余的药品应放回原试剂瓶
E.可燃性气体点燃前一定要验纯
F.使用分液漏斗前须检查其是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体.再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀.根据题意推断气体x的成分可能是( )
A.0.3mol NO2 和0.3mol NO
B.0.2mol NO2和0.1mol N2O4
C.0.1mol NO,0.2mol NO2和0.05mol N2O4
D.0.6mol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于达到平衡的可逆反应:X+YW+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X,Y,Z,W的聚集状态可能是( ) 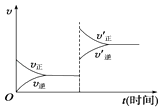
A.Z,W为气体,X,Y中之一为气体
B.Z,W中之一为气体,X,Y为非气体
C.X,Y,Z皆为气体,W为非气体
D.X,Y,Z,W皆为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,正确的是( )
A. Al2(SO4)3=2A13++3SO42- B. Ba(OH)2=Ba2++(OH-)2
C. Na2SO4=2Na++S04-2 D. Ca(N03)2=Ca2++2(N03) 2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置进行实验,图中C1、C2均为石墨棒.请回答下列问题. 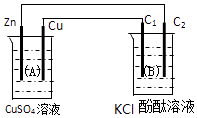
(1)锌极为极,电极反应式为:;
石墨棒C1为极,电极反应式为:;
石墨棒C2附近观察到的实验现象为;
(2)当C2极析出224mL气体(标准状态)时,锌的质量减小g,A池中溶液的质量变化(填增大、不变或减小)g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃101kPa下,①2Na(s)+ ![]() O2(g)═Na2O(s)△H1=﹣414kJ/mol,
O2(g)═Na2O(s)△H1=﹣414kJ/mol,
②2Na(s)+O2(g)═Na2O2(s)△H2=﹣511kJ/mol,
下列说法正确的是( )
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na20,随温度升高生成Na20的速率逐渐加快
D.25℃101kPa下,Na202(s)+2Na(s)═2Na20(s)△H=﹣317kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com