
下列各组物质中,因反应条件、用量、浓度等不同而发生不同化学反应的是( )
①Cu与硝酸; ②SO2与NaOH溶液; ③AlCl3溶液与KOH溶液;
④CO2与Na2SiO3溶液; ⑤Zn和硫酸; ⑥Fe和Cl2
A.除②外 B.除⑥外 C.除⑤外 D.全部
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
如右图所示,开始时,夹子处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列中的( )
A.氢氧化钠溶液、二氧化硫 B、水、氨气
C.氢氧化钠溶液、一氧化氮 D.水、二氧化氮

查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关试剂的保存方法,错误的是( )
A.浓硝酸保存在棕色试剂瓶中并放置在阴凉处 B.少量的金属钠保存在煤油中
C.液溴应保存在棕色细口瓶,并加水液封 D.新制的氯水通常保存在无色玻璃试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
在限定条件下,下列溶液中各组离子一定能大量共存的是( )
A.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
B.与Al能产生氢气的溶液:K+、SO42-、HCO3-、NH4+
C.碳酸氢钠溶液:K+、Na+、Cl-、SO42-
D.pH<7的溶液:K+、SiO32-、Na+、AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
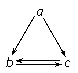
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
a | b | c | |
A | Al2O3 | AlCl3 | Al(OH)3 |
B | NH3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | Fe | FeCl2 | FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组取一定质量的FeSO4固体,利用下图装置进行实验。

| 实验过程 | 实验现象 | |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
已知:SO2 熔点–72℃,沸点–10℃;SO3熔点16.8℃,沸点44.8℃。
(1)实验③反应的离子方程式是______ _。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有_____ _气体,依据是_ _。
(3)实验④反应的离子方程式是______ _。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,原因是(用必要的文字和化学方程式解释)______ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
在元素周期表的前四周期中,有A、B、C、D四种元素.它们的原子序数依次增大.A元素原子有三个未成对电子.B元素原子次外层有八个电子;1摩尔此元素的单质与足量盐酸反应可生成1摩尔的氢气;B元素的单质不易与冷水反应.C元素的正三价离子的d轨道是半充满的.D元素易成负一价离子.
1.写出四种元素的符号.
A: B: C: D:
2.写出C元素原子的电子排布式.
3.指出四种元素的单质的晶体结构类型.
A:
B:
C:
D:
4.写出B、D两种元素所形成的化合物的电子式,此化合物的晶体在熔融时能否导电?
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石的主要成分是K2SO1·Al2(SO1)3·2Al2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:


(1)焙烧炉中发生反应的化学方程式为2Al2(SO1)3+3S 2Al2O3+9SO2,该反应的氧化剂是_______,若生成1 mol Al2O3,则转移的电子数为_______。
(2)将标况下1.12L炉气通入100mL 0.5/L NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为_______________________________________。
(3)熟料溶解时反应的离子方程式为______________。
(4)检验废渣中含有Fe2O3所需的试剂是_________。
(5)母液中溶质主要成分的化学式为__________,溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com