
NA代表阿伏加德罗常数,下列说法正确的是
| A.9 g D2O中含有的电子数为5 NA |
| B.46 g NO2和N2O4混合气体中含有原子数为3 NA |
| C.1 mol C2H6分子中共价键总数为8 NA |
| D.7.1 g C12与足量NaOH溶液反应转移的电子数为0.2 NA |
B
解析试题分析:A、水是10电子微粒,因此9 g D2O中含有的电子的物质的量=9g÷20g/mol=0.45mol,因此电子数为0.45NA,A不正确;B、NO2和N2O4的最简式相同,都是NO2,因此46 g NO2和N2O4混合气体中含有原子的物质的量=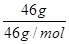 ×3=3mol,因此原子数为3 NA,B正确;C、乙烷分子中含有6个C-H键,1个C-C键,因此1 mol C2H6分子中共价键总数为7NA,C不正确;D、氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,因此氯气既是氧化剂,也是还原剂,1mol氯气转移1mol电子。7.1 g C12是7.1g÷71g/mol=0.1mol,与足量NaOH溶液反应转移的电子数为0.1NA,D不正确,答案选B。
×3=3mol,因此原子数为3 NA,B正确;C、乙烷分子中含有6个C-H键,1个C-C键,因此1 mol C2H6分子中共价键总数为7NA,C不正确;D、氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,因此氯气既是氧化剂,也是还原剂,1mol氯气转移1mol电子。7.1 g C12是7.1g÷71g/mol=0.1mol,与足量NaOH溶液反应转移的电子数为0.1NA,D不正确,答案选B。
考点:考查阿伏伽德罗常数的计算


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:单选题
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
| A.若M(甲)>M(乙),则气体体积:甲<乙 |
| B.若M(甲)<M(乙),则气体的压强:甲>乙 |
| C.若M(甲)>M(乙),则气体的摩尔体积:甲<乙 |
| D.若M(甲)<M(乙),则的分子数:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,0.05 mol·L-1Fe2(SO4)3溶液中含Fe3+数目为0.1 NA |
| B.标准状况下,22.4L甲苯中含C—H数目为8 NA |
| C.常温、常压下,1.6g O2和O3混合物中,氧原子的数目为0.1NA |
| D.0.1mol Na2O2与足量CO2反应时,转移的电子数目为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是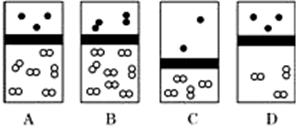
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
VmL硫酸铁溶液中含wgSO42―,取此溶液0.5VmL,用水稀释成2VmL.则稀释后的溶液中Fe3+物质的量浓度为( )
| A.125w/72v mol/L | B.250w/72v mol/L |
| C.250w/48v mol/L | D.125w/18v mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
PM2.5是指直径小于等于2.5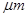 是悬浮颗粒物,其主要来源为燃煤、机动车尾气等。某实验小组将PM2.5样本用蒸馏水处理制成待测试样。测得该试样呈酸性,其各离子浓度如下表,根据表中数据可知该溶液PH为
是悬浮颗粒物,其主要来源为燃煤、机动车尾气等。某实验小组将PM2.5样本用蒸馏水处理制成待测试样。测得该试样呈酸性,其各离子浓度如下表,根据表中数据可知该溶液PH为
| 离子 | K+ | Na+ | NH4十 | 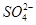 | 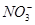 | C1— |
| 浓度/mol.L—1 | 4×l0—6 | 6×l0—6 | 2×l0—5 | 4×l0—5 | 3×l0—5 | 2×l0—5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
铜有两种常见的氧化物CuO和Cu2O。某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示。则下列分析正确的是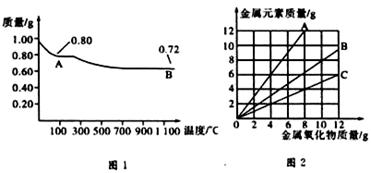
| A.图1中,A到B的过程中有0.01 mol电子发生了转移 |
| B.图1整个过程中共生成0.26 g水 |
| C.图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A |
| D.图1中A和B化学式分别为Cu2O和CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设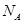 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A.1.7gH2O2中含有的中子数目为0.9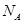 |
B.1molNa2O2固体中含离子总数为4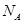 |
C.标准状况下,0.1molCl2溶于水,转移电子数目为0.1 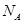 |
D.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1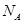 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com