
【题目】关于化学反应与能量的说法正确的是( )
A.中和反应是吸热反应
B.需要加热的反应都是吸热反应
C.断裂化学键要吸收能量
D.反应物总能量一定等于生成物总能量
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
已知:NaClO2饱和溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。Ba(ClO)2可溶于水。
利用如图所示装置进行实验。
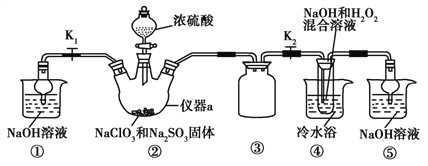
(1)仪器a的名称为____,装置①的作用是____,装置③的作用是______。
(2)装置②中产生ClO2,涉及反应的化学方程式为________________;装置④中反应生成NaClO2的化学方程式为_______________。
(3)从装置④反应后的溶液获得晶体NaClO2的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③______;④低于60 ℃干燥,得到成品。如果撤去④中的冷水浴,可能导致产品中混有的杂质是________。
(4)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作与现象是:取少量晶体溶于蒸馏水,_____________________。
(5)为了测定NaClO2粗品的纯度,取上述粗产品10.0 g溶于水配成1 L溶液,取出10 mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00 mL,试计算NaClO2粗品的纯度_____。(提示:2Na2S2O3+I2![]() Na2S4O6+2NaI)
Na2S4O6+2NaI)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年科学家首次利用X射线现测到化学反应过渡态的形成。在固体催化剂表面“抓取”CO分子和O原子,并“配对”生 成CO2分子,下列有关说法正确的是
A. CO与CO2均为酸性氧化物
B. 大量CO2的排放可导致酸雨的形成
C. CO与O形成化学键过程中有电子转移
D. 固体催化剂的使用会降低该反应的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题。
(1)乙烯的电子式为______________;
(2)当0.2mol烃A在足量氧气中完全燃烧时生成CO2和H2O各1.2mol,催化加氢后生成
2,2-二甲基丁烷,则A的结构简式为______________________________。
(3)某烃1mol与2molHCl完全加成,生成的氯代烷最多还可以与4molCl2反应,则该烃的结构简式为______________________。
(4)相对分子质量为72且沸点最低的烷烃的结构简式_______________________;
(5)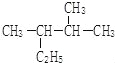 的名称(系统命名法)_______________________。
的名称(系统命名法)_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学观或化学研究方法的叙述中,错误的是( )
A.在化工生产中应遵循“绿色化学”的思想
B.在过渡元素中寻找优良的催化剂
C.在元素周期表的金属和非金属分界线附近寻找半导体材料
D.根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是立方烷(C8H8)的球棍模型,下列有关说法不正确的是( )

A.它的一氯代物只有一种同分异构体
B.它的二氯代物有三种同分异构体
C.它与苯乙烯(C6H5-CH=CH2)互为同分异构体
D.它是一种不饱和烃,既能发生取代反应,又能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离方法不正确的是 ( )
A.用过滤的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.用酒精萃取碘水中的碘
D.用淘洗的方法从沙里淘金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业含铬(Cr)废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀.废水pH与Cr2O72-转化为Cr3+的关系如图1,实验室模拟工业电解法处理含铬废水的装置如图2:
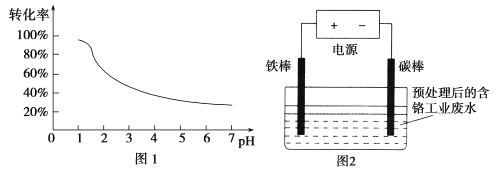
有关数据如下表所示:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cr(OH)3 |
开始沉淀的pH | 1.9 | 7.5 | 4.3 |
完全沉淀的pH | 3.4 | 9.7 | 7.6 |
请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是 。
(2)电解过程中阳极质量减小,阴极有气体产生,写出两极的电极反应式:
阳极 ,阴极 。
(3)写出Cr2O72-转化为Cr3+的离子方程式: 。
(4)每处理1molCr2O72-,外电路中转移 mol电子。
(5)电解过程中解液的pH (填增大、减小或不变)
(6)处理过程中,当废水颜色不再发生明显变化时,切断电源,取出电极。此时,溶液中的阳离子有Fe2+、Fe3+、Cr3+,若想用调节pH的方法得到纯净的Cr(OH)3沉淀,应先向溶液中加入适量的 ,再调节pH= ,过滤后继续调节pH= 8。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KNO3和Cu(NO3)2的混合溶液200mL,其中c(NO3-)=2mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24L气体(标准状况),假设电解后溶液体积不变,下列说法正确的是( )
A.原混合溶液中c(K+)=0.5mol·L-1
B.电解得到的Cu的物质的量为0.2mol
C.上述电解过程中共转移0.4mol电子
D.电解后溶液中c(H+)=2mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com