
【题目】下列说法不正确的是( )
A. 乙酸乙酯中混有乙酸可用NaOH溶液除去
B. 乙醇、乙酸都可以与金属钠反应生成氢气
C. 乙醛可以催化氧化为乙酸
D. 乙醇与乙酸反应可以制备乙酸乙酯
【答案】A
【解析】A. 乙酸乙酯中混有乙酸,因乙酸乙酯在NaOH溶液中可以水解生成乙酸钠和乙醇,故不能用NaOH溶液除去乙酸乙酯中混有的乙酸,可以用饱和的Na2CO3溶液,故A错误;
B. 乙醇与金属钠发生反应:2Na+2CH3CH2OH ![]() 2CH3CH2ONa+H2↑,乙酸与金属钠发生反应:2Na+2CH3COOH
2CH3CH2ONa+H2↑,乙酸与金属钠发生反应:2Na+2CH3COOH![]() 2CH3COONa+H2↑,乙醇、乙酸都可以与金属钠反应生成氢气,故B正确;
2CH3COONa+H2↑,乙醇、乙酸都可以与金属钠反应生成氢气,故B正确;
C. 乙醛可以在催化剂作用下发生氧化反应生成乙酸,2CH3CHO+O2![]() 2CH3COOH,故C正确;
2CH3COOH,故C正确;
D. 乙醇与乙酸可以发生酯化反应生成乙酸乙酯,CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O,故D正确;
CH3COOCH2CH3+H2O,故D正确;
故答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】把铁和铜加入到氯化铁、氯化亚铁和氯化铜的混合溶液中,反应后铁有剩余则
A.溶液中有Fe2+、Cu2+
B.剩下的固体是Fe和Cu
C.溶液中有Fe3+、Fe2+
D.剩下的固体是Fe,无Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氧化二钒广泛用于冶金、化工等行业,主要用于冶炼钒铁.用作合金添加剂,占五氧化二钒总消耗量的80%以上,其次是用作有机化工的催化剂,为了增加V2O5的利用率,我们从废钒催化剂(主要成分V2O5,VOSO4,K2SO4,SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:

部分含钒物质在水中的溶解性如下,回答下列问题:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解牲 | 可溶 | 难溶 | 难溶 | 易溶 |
(l)①中废渣的主要成分是____;①中V2O5发生反应的离子方程式为_____________。
(2)②,③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):R2(SO4)n(水层)+2nHA(有机层)![]() 2RA(有机层)+nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是________________;实验室进行萃取操作主要使用的玻璃仪器为________________。
2RA(有机层)+nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是________________;实验室进行萃取操作主要使用的玻璃仪器为________________。
(3)实验室用的原料中V2O5占6%(原料中的所有钒已换算成V2O5)。取l00g该废钒催化剂按工业生产的步骤进行实验,当加入100 mL0.1mol/L的KC1O3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该实验中钒的回收率是____(己知V2O5的相对分子质量为182)。
(4) 25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间的关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 | 89.3 |
试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为_________;若钒沉淀率为93.1%时不产生Fe( OH)3沉淀,则此时溶液中c(Fe3+)=_________。(已知:25℃时k[Fe(OH)3]=2.6×l0-39.)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中,下列离子能大量共存的是
A. Fe2+、Na+、SO42-、Cl-
B. Na+、Ba2+、CO32-、NO3-
C. Cu2+、K+、Cl-、SO42-
D. K+、Na+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
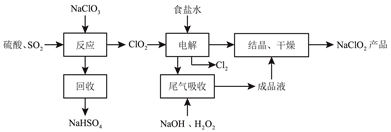
已知:亚氯酸钠在温度高于80℃时分解。下列说法不正确的是( )
A. “反应”步骤中生成ClO2的化学方程式是:2NaClO3+SO2+H2SO4===2NaHSO4+2ClO2
B. 电解食盐水的阴极产物是NaOH和H2
C. ClO2尾气吸收时氧化剂和还原剂的物质的量之比为1:1
D. 从NaClO2溶液中得到NaClO2产品,应采用减压蒸发的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在一固定容积的密闭容器中发生反应:A(g)+B(g)![]() C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是

A. T℃时,该反应的平衡常数值为4
B. c点没有达到平衡,此时反应向逆向进行
C. 若c点为平衡点,则此时容器内的温度高于T℃
D. T℃时,直线cd上的点均为平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题成为人类共同关注的问题,欧洲很多国家提出了燃油车2036年停产时间表。也有专家提出燃油车远未到穷途末路,只要解决燃油汽车排放的尾气中的SO2、CO和NO污染问题就还有很长的生命,请回答以下问题:
(1)在汽车尾气管中加装催化剂成为汽车尾气治理的常用方法,已知:
①N2(g)+ O2(g)=2NO(g) △H=180.5 kJ/mol
②2CO(g)+ O2(g)=2CO2(g) △H=-566kJ/mol
写出NO(g)与CO(g)在催化剂作用下转化成N2(g)和CO2(g)的热化学方程式________________________。
(2)汽车尾气中的少量NO2也可以和CO反应生成N2(g)和CO2(g),热化学方程式为:
2NO2(g)+4CO(g)= N2(g)+4CO2(g) ,ΔH=QkJ·mol-1,试判断Q_______0(填“>”或“<”或“=”)。理由是_________________________________________
(3)除了汽车尾气产生的污染外,工业尾气及北方冬季燃煤产生SO2的污染治理也非常重要,可模仿工业上用2SO2(g )+O2(g) ![]() 2SO3(g)以制取硫酸,现在一容积固定为10L的密闭容器中进行该反应,现测得如下数据:
2SO3(g)以制取硫酸,现在一容积固定为10L的密闭容器中进行该反应,现测得如下数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
SO2 | O2 | SO2 | |||
1 | 550 | 4 | 2 | 0.4 | 9 |
2 | 650 | 2 | 1 | 0.4 | 3 |
3 | 650 | a | b | c | t |