
被誉为“太空金属”的钛,在室温下,不与水、稀硫酸、稀盐酸和稀硝酸作用,但易溶于氢氟酸,其原因可能是( )
A.氢氟酸的酸性比其他酸强
B.氢氟酸的氧化性比其它酸强
C.钛离子易与氟离子形成可溶性难电离物质
D.氢氟酸的还原性比其它酸强
科目:高中化学 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:选择题
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)  2CO2(g)+S(l) △H < 0,若反应在恒容的密闭容器中进行,下列有关说法不正确的是
2CO2(g)+S(l) △H < 0,若反应在恒容的密闭容器中进行,下列有关说法不正确的是
A.其它条件不变,使用不同催化剂,该反应的平衡常数不变
B.平衡前,随着反应的进行,容器内压强始终不变
C.平衡时,其它条件不变,分离出少量的硫,正反应速率不变
D.平衡时,其他条件不变,升高温度可使反应速率加快,平衡常数减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南国兴中学高二上第三次月考化学试卷(解析版) 题型:选择题
下列过程中所发生的化学变化属于加成反应的是
A.乙烯通入酸性高锰酸钾溶液中 B.光照射甲烷与氯气的混合气体
C.在镍作催化剂的条件下,苯与氢气反应 D.苯与液溴混合后撒入铁粉
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北衡水冀州中学高二上月考三化学试卷(解析版) 题型:选择题
如图所示,X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味的气体放出,符合这一情况的是( )
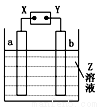
a极板 | b极板 | X电极 | Z | |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2[XK] |
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期月考(三)化学试卷(解析版) 题型:实验题
CoCl2•6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如下:
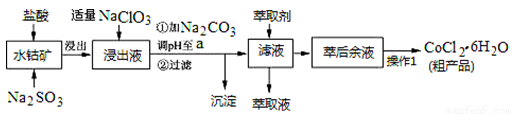
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等,还原性Fe2+>Cl->Co2+;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
回答下列问题:
(1)写出浸出过程中Co2O3发生反应的离子方程式 。
(2)写出NaClO3发生反应的主要离子方程式 ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 。
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为 、 。
(4)“操作1”中包含的基本实验操作,它们依次是 和过滤、减压烘干。
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是 ;其使用的最佳pH范围是 。.
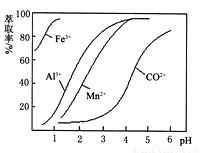
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
查看答案和解析>>
科目:高中化学 来源:2016届四川省成都市高三上学期期中考试化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA
B.电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数为0.2NA
C.常温下,1.0L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1N
D.将100mL0.1mol·L -1 的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期期中测试化学试卷(解析版) 题型:选择题
有可逆反应aA(g)+bB(g)  cC(g)+dD(g) ΔH,试根据下图下列判断错误的是
cC(g)+dD(g) ΔH,试根据下图下列判断错误的是
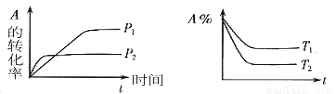
A.压强P1<P2 B.a+b<c+d C. T1<T2 D.△H<0。
查看答案和解析>>
科目:高中化学 来源:2016届山东省济宁市高三上学期期中考试化学试卷(解析版) 题型:实验题
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。工业流程图如下:
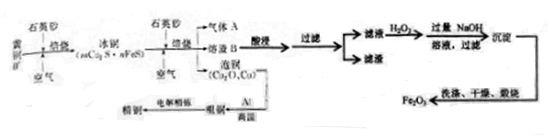
(1)冶炼铜的总反应可看做:8CuFeS2+21O2  8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__ __(填元素符号),1molCuFeS2参与反应转移电子的物质的量为 mol;
8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__ __(填元素符号),1molCuFeS2参与反应转移电子的物质的量为 mol;
(2)上述冶炼过程产生大量气体A。下列处理方案中合理的是 (填代号);
A.高空排放
B.用于制备硫酸
C.用纯碱溶液吸收制Na2SO4
D.用浓硫酸吸收
验证气体A的主要成分是SO2的方法是 ;
(3)炉渣B(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。
A.加入H2O2发生反应的离子方程式是 ;
B.除去Al3+的离子方程式是 ;
(4)选用提供的试剂,设计实验验证炉渣B中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 ;
证明炉渣中含有FeO的实验现象为 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省澧县、桃源、益阳三校高三上学期联考化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值,下列说法正确的是
A.Na2O2与水反应制O2,每生成0.25molO2转移电子数为1NA
B.等物质的量的N2和CO所含原子数均为2NA
C.在标准状况下,11.2L HCHO所含的分子数约为0.5NA
D.1molSO2与足量的O2反应,转移的电子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com