
实验测得:298 K、101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;
1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是 ( )
①CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=890.3 kJ·mol-1
②CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.3 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
A.仅有② B.仅有②④
C.仅有②③④ D.全部符合要求
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
环境问题正成为21世纪世界的热点问题,请填写下列空白。
①在二氧化碳、二氧化硫、二氧化氮、氟氯烃中,能造成臭氧层空洞的物质有_______和二氧化氮;能造成酸雨的主要因素是__ __和二氧化硫含量的增加。
②高铁酸钾(K2FeO4)是新型、高效的水处理剂,其氧化性比氯气、臭氧等更强,遇水易变化,在水处理过程中高铁酸钾被还原为Fe3+。高铁酸钾除能消毒、杀菌外,还能除去水中的悬浮颗粒的原因是___ _____(用化学方程式表示)。
③废水中的Cr3+、Ag+、Hg2+等常采用 法消除污染
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的制取,实验操作正确的是
A.将CuCl2溶液置于蒸发皿中加热蒸干,可制取无水CuCl2固体
B.将NH4HCO3饱和溶液置于蒸发皿中加热蒸于,可制取NH4HCO3固体
C.向FeCl3饱和溶液中缓慢滴入过量氨水加热,可制取Fe(0H)3胶体
D.向电石中缓慢滴入饱和食盐水,可制取C2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一个化学过程的示意图。
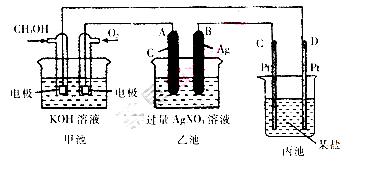
(l)请回答图中甲池是一装置,其中OH-移向一极(填“CH3OH”或“O2”)
(2)写出通入CH3OH的电极的电极反应式_________。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为_________极(填“A”或“B”),并写出此电极反应的电极反应式____________。
(4)乙池中反应的离子方程式为____________。
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是________(若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是一(填序号). A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于能量的变化及反应热的说法中正确是 ( )
A.任何化学反应都有反应热
B.有些化学键断裂时吸收能量,有些化学键断裂时放出能量
C.新化学键的形 成不一定放出能量
成不一定放出能量
D.有热量变化的反应一定有化学键的断裂与形成
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2SO4(aq)与Ba(OH)2(aq)反应的ΔH=-1 584.2 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-55.6 kJ·mol-1。则生成BaSO4(s)的反应热等于 ( )
A.-1 528.6 kJ·mol-1 B.-1 473 kJ·mol-1
C.1 473 kJ·mol-1 D.1 528.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:(ⅰ)CO(g)+2H2(g)===CH3OH(g)
ΔH1=-90.1 kJ·mol-1
(ⅱ)CO2(g)+3H2(g)===CH3OH(g)+H2O(g)
ΔH2=-49.0 kJ·mol-1
水煤气变换反应:(ⅲ)CO(g)+H2O(g)===CO2(g)+H2(g)
ΔH3=-41.1 kJ·mol-1
二甲醚合成反应:(ⅳ)2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ·mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
2CO(g)+4H2(g)===2CH4(g)+O2(g)
ΔH=71 kJ·mol-1;CO(g)+2H2(g)===CH3OH(l) ΔH=-90.5 kJ·mol-1。
已知CH4(g)的燃烧热为-890 kJ·mol-1,则CH3OH(l)的燃烧热ΔH为 ( )
A.-1 528 kJ·mol-1 B.-764 kJ·mol-1
C.-382 kJ·mol-1 D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为:
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为:
CH3—CH2—O—CH2—CH3
其核磁共振谱中给出的峰值(信号)有两个,如图所示:
(1) (4分)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是 (多选扣分)。
A.CH3CH3 B. CH3COOH C. CH3COOCH3 D. CH3OCH3
 (2) (4分)化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如右图所示,则A的结构简式为: ,请预测B的核磁共振氢谱上有 个峰(信号)。
(2) (4分)化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如右图所示,则A的结构简式为: ,请预测B的核磁共振氢谱上有 个峰(信号)。
(3)(4分)用核磁共振氢谱的方法来研究C2H6O的结构,
简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com