
分析 利用40mL 5mol/L的盐酸的物质的量,根据反应的化学方程式,计算参加反应的碳酸钙的质量,生成二氧化碳的物质的量,然后根据V=nVm,进行计算解答.
解答 解:40mL 5mol/L的盐酸的物质的量为:40×5×10-3mol=0.2mol,设生成的CO2在标准状况下的体积为VL,消耗CaCO3的质量为xg,
由反应方程式CaCO3+2HCl═CaCl2+H2O+CO2↑
100g 2mol 22.4L
xg 0.2mol VL
所以$\frac{100g}{xg}=\frac{2mol}{0.2mol}=\frac{22.4L}{VL}$
解之得:x=10g,V=2.24L,
答:(1)生成的CO2在标准状况下的体积为2.24L.
(2)消耗CaCO3的质量为10g.
点评 本题主要考查了质量守恒定律的应用和根据化学方程式进行有关的计算,要注意解题的步骤和计算结果的准确性,此题难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 蔗糖和麦芽糖均能发生水解反应和银镜反应 | |
| B. | 植物油可用于萃取碘水中的碘 | |
| C. | 面粉、牛油、丝绸完全燃烧都只生成CO2和H2O | |
| D. | 用渗析的方法不能对鸡蛋白和淀粉的混合溶液进行分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
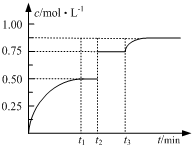 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应:
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应:| A. | 若t1=2,则反应在0~2 min内的平均速率为v(A)=0.50 mol•(L•min)-1 | |
| B. | 若t3时刻升高了温度,则该反应的△H>0 | |
| C. | 若t1时刻后向体系中加入A、B、C各1 mol,则υ(正)>υ(逆) | |
| D. | 温度不变,若起始向容器中加入1 mol A、1 mol B、2 mol D,则达平衡时A的转化率小于50% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “胃得乐”(主要成分为碳酸镁)是一种抗酸药) | |
| B. | 鸦片、吗啡、海洛因等这些物质属于毒品 | |
| C. | 青霉素能抑制细菌细胞壁的生长,致使细菌因细胞破裂而死亡 | |
| D. | “阿司匹林”是一种重要的抗生素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | △H1-△H2<0 | |
| B. | 反应②为放热反应 | |
| C. | 3CH3OCH3(g)=2CH3CH=CH2(g)+3H2O(g)△H=-103.0 kJ•mol-1 | |
| D. | 3CO(g)+6H2(g)=CH3CH=CH2(g)+3H2O(g)△H=-301.3kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol•L-1 | B. | 0.15mol•L-1 | C. | 0.04mol•L-1 | D. | 0.4mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com