
将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应:
I2(g) + H2(g) 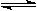 2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
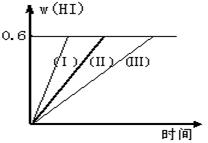
(1)达平衡时,I2(g)的物质的量浓度为 写出该反应的平衡常数表达式 _____________________________________。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是 ,则乙条件可能是 。
(填入下列条件的序号)
①恒容条件下,升高温度; ②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积; ④恒温条件下,扩大反应容器体积; ⑤恒温恒容条件下,加入适当催化剂。
(1) 0.05mol/L;K=[HI]2/[H2][I2] (2) 3、5;4
【解析】
试题分析:(1)由于该反应前后气体体积不变,所以根据图像可知,平衡时HI的物质的量是3mol×0.6=1.8mol,则消耗单质碘的物质的量是0.9mol,所以平衡时I2(g)的物质的量浓度为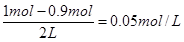 ;化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此根据反应的化学方程式可知,该反应的平衡常数K=[HI]2/[H2][I2]。
;化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此根据反应的化学方程式可知,该反应的平衡常数K=[HI]2/[H2][I2]。
(2)曲线(Ⅰ)和曲线(Ⅱ)相比,HI的含量不变,即平衡状态不变,但到达平衡的时间减少。这说明反应速率加快,所以改变的条件应该是恒温条件下,缩小反应容器体积或恒温恒容条件下,加入适当催化剂,答案选③⑤;曲线(Ⅲ) 和曲线(Ⅱ)相比,HI的含量不变,即平衡状态不变,但到达平衡的时间增加。这说明反应速率降低,所以改变的条件应该是恒温条件下,扩大反应容器体积,答案选④。
考点:考查可逆反应的有关计算、平衡常数以及外界条件对平衡状态的影响等
点评:本题是高考中的常见题型,属于中等难度的试题,试题基础性强,难易适中。本题主要是检验学生对基础知识的理解掌握程度,以及图像识别、分析、归纳问题的能力,本题学生不难得分。


科目:高中化学 来源: 题型:
将1 mol I2(g)和2 mol H2置于某![]() 2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。
2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。

(1)达到平衡时,I2(g)的物质的量浓度为______________mol·L-1。
(2)若改变反应条件,在甲条件下w(HI)的变化如图曲线(Ⅱ)所示,在乙条件下w(HI)的变化如图曲线(Ⅲ)所示。则甲条件可能是______________,乙条件可能是______________。(填入下列条件的序号)
①恒容条件下,升高温度 ②恒容条件下,降低温度 ③恒温条件下,缩小反应容器体积 ④恒温条件下,扩大反应容器体积 ⑤恒温恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
I2(g)+H2(g) ![]() 2HI(g);ΔH<0,并达到平衡。HI的体积分数φ(HI)随时间变化如下图中曲线(Ⅱ)所示:
2HI(g);ΔH<0,并达到平衡。HI的体积分数φ(HI)随时间变化如下图中曲线(Ⅱ)所示:

(1)达平衡时,I2(g)的物质的量浓度为_______ mol·L -1。
(2)若改变反应条件,在某条件下φ(HI)的变化如曲线(Ⅰ)所示,则该条件可能是______(填下列条件的序号)。?
①恒容条件下,升高温度?
②恒容条件下,降低温度?
③恒温条件下,缩小反应容器体积?
④恒温条件下,扩大反应容器体积?
⑤恒温、恒容条件下,加入适当催化剂?
(3)若保持温度不变,在另一相同的2 L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c应满足的关系为_______(用一个含a、b、c的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
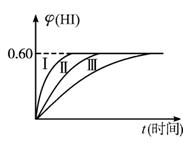
图1-2-9
(1)达到平衡时,I2(g)的物质的量浓度为___________mol·L-1。
(2)若改变反应条件,在甲条件下φ(HI)的变化如图中曲线(Ⅰ)所示,在乙条件下φ(HI)的变化如图中曲线(Ⅲ)所示,则甲条件可能是___________,乙条件可能是___________ (填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下降低温度
③恒温条件下,缩小反应容器的体积
④恒温条件下,扩大反应容器的体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2 L密闭容器中加a mol I2(g),b mol H2和c mol HI(a,b,c均大于0),发生反应达到平衡时,HI的体积分数仍为0.60,则a,b,c的关系是___________。
查看答案和解析>>
科目:高中化学 来源:2012届云南省高二下学期期中考试化学试卷 题型:填空题
(12分)将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应: H2(g) + I2(g)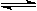 2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:

(1)达平衡时,I2(g)的物质的量浓度为 。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是 ,则乙条件可能是 。
(填入下列条件的序号)[来源:学#科#网Z#X#X#K]
①恒容条件下,升高温度;②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积;④恒温条件下,扩大反应容器体积;⑤恒温恒容条件下,加入适当催化剂。
(3)若保持温度不变,在另一个相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,则a、b、c的关系是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com