
����Ŀ����ͼ1Ϊʵ������ȡ������ʵ��װ�á�
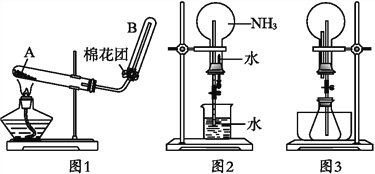
��1��д��A����������Ӧ�Ļ�ѧ����ʽ_______________________��Ҫ�ռ�����İ�����������____________________���������
��2�����ռ�����ʱ�Թܿ�����������___________��
��3��һλѧ�����Ƶõİ���,��ͼ2װ�ý�����Ȫʵ��,��ƿ�ѳ�������İ���,������Ȫʵ��IJ�����___________��
��4����һѧ������˼��������Ȫ����������,�����ͼ3װ�á���������ƿ�зֱ������������������,��Ӧ���ܲ�����Ȫ����___________��
A.CaCO3��ĩ��Ũ���� B.NH4HCO3��Һ��ϡNaOH��Һ
C.HCl��AgNO3��Һ D.HCl����ɫ��̪��Һ
��ͬѧ������ƿ�м���ƾ�,ˮ���м�����ˮ��,�ټ�����������������,���Ҳ��������Ȫ��ˮ���м�������ʿ�����___��
A.����� B.ʳ�� C.Ũ���� D.����ͭ
��5�����鰱���ѳ����Թ�B�ķ�����______________��
��6�����Ƶñ�״���µİ���2.24L����Ӧ��������Ҫ��ʯ��______g
���𰸡� 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O ��ʯ�ң������NaOH��CaO�� ����������Ķ���,��֤�Թ������ռ������� ����Ƥ�ܵļ���,��ѹ��ͷ�ιܵĽ�ͷ,ʹ������ˮ������ƿ A C ��ʪ�����ɫʯ����ֽ����B�Թܿڣ���ֽ����֤������������������Ҳ���֣� 3.7g
CaCl2+2NH3��+2H2O ��ʯ�ң������NaOH��CaO�� ����������Ķ���,��֤�Թ������ռ������� ����Ƥ�ܵļ���,��ѹ��ͷ�ιܵĽ�ͷ,ʹ������ˮ������ƿ A C ��ʪ�����ɫʯ����ֽ����B�Թܿڣ���ֽ����֤������������������Ҳ���֣� 3.7g
����������1�����õ��ǹ�+�̻�ϼ��������ķ����������Ȼ�狀��������ƹ����ϼ�����NH3���Ȼ�����������Ʒ�Ӧ�����Ȼ��ơ�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O��Ҫ�ռ�����İ����������ü�ʯ�ң������NaOH��CaO�������������2���ռ������õ��������ſ��������Թܿ����������Ǽ��ٰ���������Ķ������ӿ��ռ������ʣ�ͬʱ��֤�Թ������ռ�����������3��������������ˮ�������ֹˮ�У���������ˮ����ƿ��ѹǿѸ�ټ�С�����γ���Ȫ���ʴ�Ϊ������Ƥ�ܵļ��ӣ���ѹ��ͷ�ιܵĽ�ͷ��ʹ������ˮ������ƿ����4��CaCO3��ĩ��Ũ���ᷴӦ��������������̼��ʹ��ƿ��ѹǿ�����γ���Ȫ��ѡ��A��ȷ��B��NH4HCO3��Һ��ϡNaOH��Һ�����������壬�����γ���Ȫ��ѡ��B����C��HCl��AgNO3��Һ�����������壬�����γ���Ȫ��ѡ��C����D��HCl�ͷ�̪��Һ�����������壬�����γ���Ȫ��ѡ��D����ѡA��
CaCl2+2NH3��+2H2O��Ҫ�ռ�����İ����������ü�ʯ�ң������NaOH��CaO�������������2���ռ������õ��������ſ��������Թܿ����������Ǽ��ٰ���������Ķ������ӿ��ռ������ʣ�ͬʱ��֤�Թ������ռ�����������3��������������ˮ�������ֹˮ�У���������ˮ����ƿ��ѹǿѸ�ټ�С�����γ���Ȫ���ʴ�Ϊ������Ƥ�ܵļ��ӣ���ѹ��ͷ�ιܵĽ�ͷ��ʹ������ˮ������ƿ����4��CaCO3��ĩ��Ũ���ᷴӦ��������������̼��ʹ��ƿ��ѹǿ�����γ���Ȫ��ѡ��A��ȷ��B��NH4HCO3��Һ��ϡNaOH��Һ�����������壬�����γ���Ȫ��ѡ��B����C��HCl��AgNO3��Һ�����������壬�����γ���Ȫ��ѡ��C����D��HCl�ͷ�̪��Һ�����������壬�����γ���Ȫ��ѡ��D����ѡA��
��ƿ��װ�оƾ����ӷ���Ҫ�γ���Ȫ��Ӧʹ��ƿ��ѹǿ������������Ӧ�ų��������ȣ�Ũ������ˮ��ϡ�ͣ��ͷų��������ȣ�ʹ��ƿ�е��Ҵ��ӷ���ѹǿ�����γ���Ȫ�����������ʶ����ܴﵽ����ˮ���ų��������ȵ�Ŀ�ģ�ֻ��C���ϣ���ѡC����5�����鰱���ѳ����Թ�B�ķ�������ʪ��ĺ�ɫʯ����ֽ����B�Թܿڣ���ֽ����֤����������6�����Ƶñ�״���µİ���2.24L�����ݷ�Ӧ2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O����������Ҫ��ʯ��
CaCl2+2NH3��+2H2O����������Ҫ��ʯ��![]() g��
g��


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������2molSO2�������У���ȷ���ǣ� ��
A.���Ϊ44.8 LB.����4mol��ԭ��
C.������Ϊ6.02��1023D.Ħ������Ϊ128 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС������֤��Ӧ��Fe+2Ag+=Fe2++2Ag����ʵ���м�Fe3+ �� ���ֺ�̽���������£�
�������ữ��0.05molL��1��������Һ��pH��2���м���������ۣ�������ã��ձ��ײ��к�ɫ���壬��Һ�ʻ�ɫ��
��1���������
��ȡ������ɫ���壬ϴ�Ӻ��������������֤����ɫ�����к���Ag��
��ȡ�ϲ���Һ���μ�K3[Fe��CN��6]��Һ��������ɫ������˵����Һ�к��� ��
��2����ԡ���Һ�ʻ�ɫ��������Ϊ��Һ����Fe3+ �� ����Ϊ���۹���ʱ��������Fe3+ �� �����ݵ�ԭ�����������ӷ���ʽ��ʾ����������ֹ۵����ʵ�飺
��ȡ�ϲ���Һ���μ�KSCN��Һ����Һ��죬֤ʵ�˼IJ²⣮ͬʱ�����а�ɫ��������������Һ��ɫ��dz��������������ȡ��ʱ���йأ��Ա�ʵ���¼���£�
��� | ȡ��ʱ��/min | ���� |
�� | 3 | ����������ɫ��������Һ�ʺ�ɫ |
�� | 30 | ������ɫ��������3minʱ��С����Һ��ɫ��3minʱ���� |
�� | 120 | ������ɫ��������30minʱ��С����Һ��ɫ��3 0minʱ��dz |
�����ϣ�Ag+��SCN�����ɰ�ɫ����AgSCN��
�ڶ�Fe3+������ԭ���������¼��裺
����a�����������۱����������㣬�ܲ���Fe3+��
����b�������д���O2 �� �����������ӷ���ʽ��ʾ�����ɲ���Fe3+��
����c��������Һ��NO3�����������ԣ��ɲ���Fe3+��
����d�����������ж���Һ�д���Ag+ �� �ɲ���Fe3+ ��
������ʵ����֤ʵ����a��b��c���Dz���Fe3+����Ҫԭ��ʵ����֤ʵ����d������
ʵ����������ữ����Һ��pH��2���м���������ۣ�������ã���ͬʱ��ȡ�ϲ���Һ�μ�KSCN��Һ��3minʱ��Һ��dz��ɫ��30min����Һ������ɫ��
ʵ���װ����ͼ�����м���Һ�� �� ���������� �� 
��3������ʵ������Ϸ���ʽ�Ʋ�ʵ�颡������Fe3+Ũ�ȱ仯��ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬλ��,����Ȼ���и�ռһ��,��֪��ԭ�ӵ�������Ϊ35.��Ľ������ԭ������Ϊ80,���������ͬλ�ص���������.
A.19��81
B.45��46
C.44��45
D.44��46
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�����Ŀ��
��1��30%��H2SO4��50%��H2SO4��������Ϻ�������Һ����������������ڡ�����С�ڡ����ڡ���40%������������ϣ���Ϻ���Һ����������������ڡ�����С�ڡ����ڡ���40%��
��2����֪98%��ŨH2SO4�����ʵ���Ũ��Ϊ18.4molL��1 �� ���ж�49%��H2SO4�����ʵ���Ũ��������ڡ�����С�ڡ����ڡ���9.2molL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.������ѧ֪ʶ���ش�����������
��1��Ԫ�����ڱ�1��20��Ԫ���У���������ǿ��Ԫ����______(��Ԫ�ط��ţ���ͬ)������ϡ���������_________���ǽ�������ǿ��Ԫ�������ڱ��е�λ����__________________��
��2����֪NO2��N2O4֮�䷢�����淴Ӧ:2NO2(g)(����ɫ)![]() N2O4(g)(��ɫ)����װ��NO2��N2O4����������ƿ������ˮ�У��۲쵽��������_______�������������ԭ����________��
N2O4(g)(��ɫ)����װ��NO2��N2O4����������ƿ������ˮ�У��۲쵽��������_______�������������ԭ����________��
��3��һ�������£���2L�����ܱ������а������1:3����4.48L(��״��)N2��H2�Ļ�����壬������ӦN2(g)+3H2(g)![]() 2NH3(g)��5minʱ��Ӧ�ﵽƽ��״̬�����c(N2)=0.02mol/L��
2NH3(g)��5minʱ��Ӧ�ﵽƽ��״̬�����c(N2)=0.02mol/L��
��0��5min�ڣ�v(NH3)=_______________��
������������֤��������Ӧ�ﵽƽ��״̬����________(�����)��
a.V(H2)=3v(N2)
b.������ѹǿ���ֲ���
c.ÿ����ImolN2��ͬʱ����2molNH3
d.N2��H2��NH3�����ʵ���Ũ�Ȳ��ٱ仯
II.���ֶ�����Ԫ��A��B��C��D��E��ԭ��������������A��Cͬ�壬B��Dͬ�壬C�ļ����Ӻ�B�ļ����Ӿ�����ͬ�ĵ��Ӳ�ṹ��A��B��D��E�����γɹ����ͻ����A��B�γɵĻ�������ˮ�гʼ��ԣ�C��E�γɵĻ��������������ӵĸ�����Ϊ1:1���ش�����������
��1������Ԫ���У�ԭ�Ӱ뾶������______(��Ԫ������)���ǽ�������ǿԪ�ص���_________��
��2����Ԫ��A�ֱ��Ԫ��B��D��E���γɵĹ����ͻ������У����ȶ���������_____(�û�ѧʽ��ʾ)��
��3��Ԫ��A��E�γɵĻ�������Ԫ��A��B�γɵĻ����ﷴӦ������ĵ���ʽΪ______�����д��ڵĻ�ѧ������Ϊ______________��
��4��E���ӵĽṹʾ��ͼ��____________��Ԫ��D����������ˮ����Ļ�ѧʽΪ_____��
��5������E��ˮ��Ӧ�����ӷ���ʽΪ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ������Ҫ����500mL 0.10mol/L Na2CO3��Һ��
��1�����貣�������У����������ձ���100mL��Ͳ��
��2��ʵ��ʱͼ����ʾ�������Ⱥ�˳��Ϊ�����ţ�
��3�������ƹ����У����в�����������ҺŨ������Ӱ�죿���ƫ�ߡ�����ƫ�͡�����Ӱ�족��
�ٳ���ʱ���á��������
��ת����Һ��û��ϴ���ձ��Ͳ�����
��������ƿ��ˮ����ʱ����Һ��
��ҡ�Ⱥ�Һ���½����ټ�ˮ���̶���
��4������Na2CO3���������Ϊg��������Ũ��Һϡ�ͣ���Ҫ��ȡ2mol/L Na2CO3��ҺmL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij֬���廯����A����Է�������Ϊ118������C����������Ϊ41%��HΪ5%��OΪ54%��������A����̼��������Һ��Ӧ�ų����壬Ҳ��������������ͭ����Һ��Ӧ����ש��ɫ����������������A�Ĵ��ǻ�ͬ���칹���У� ��
A.2��
B.3��
C.4��
D.5��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com