
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某些馆的外壳使用非晶硅薄膜,以充分利用太阳能 | |
| B. | 世博会期间,利用可降解的“主米塑料”替代一次性饭盒,可防止产生白色污染 | |
| C. | 世博会中国馆“东方之冠”使用的钢筋混凝土属于高分子化合物 | |
| D. | 世博停车场安装催化光解设施,可将汽车尾气中的CO和NO 转化为无毒气体CO2和N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物 | |
| B. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 | |
| C. | 与相同浓度的酸反应的速率:Na2CO3<NaHCO3 | |
| D. | Na着火时可用泡沫灭火器灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
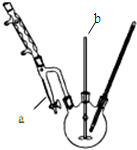 塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂.反应原理为:
塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂.反应原理为: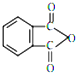 +2CH3CH2CH2CH2OH→
+2CH3CH2CH2CH2OH→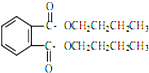 +H2O
+H2O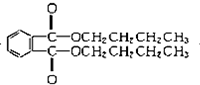 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$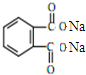 +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com