
����Ŀ��ij�л���M����C��H��O����Ԫ����ɣ���һ����������M����ת��Ϊ�л���X��W��N��ת���ϵ��ͼ�� 
��֪��
��X�Ǻܳ�����ʯ�ͻ����Ļ���ԭ�ϣ�Ҳ��һ��ֲ���������ڼ���
��R��CHO ![]() R��COOH
R��COOH
�� 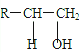
![]() R��CH=CH2+H2O��������ȥ��Ӧ
R��CH=CH2+H2O��������ȥ��Ӧ
��1��д��X��Y��Z�Ľṹ��ʽX Y Z
��2��д��ʵ������ת���Ļ�ѧ����ʽ����ע����Ӧ���� M��X
M��W
X��M
M��N ��
���𰸡�
��1��CH2=CH2�� CH3CH2Cl�� CH3COOH
��2��CH3CH2OH ![]() CH2=CH2��+H2O,��ȥ��Ӧ��2CH3CH2OH+O2
CH2=CH2��+H2O,��ȥ��Ӧ��2CH3CH2OH+O2![]() 2CH3CHO+2H2O,������Ӧ�� CH2=CH2+H2O
2CH3CHO+2H2O,������Ӧ�� CH2=CH2+H2O ![]() CH3CH2OH,�ӳɷ�Ӧ�� CH3COOH+CH3CH2OH
CH3CH2OH,�ӳɷ�Ӧ�� CH3COOH+CH3CH2OH ![]() CH3COOC2H5+H2O,������Ӧ
CH3COOC2H5+H2O,������Ӧ
���������⣺��1��ͨ�����Ϸ���֪��X��Y��Z�Ľṹ��ʽ�ֱ����Ҵ�CH3CH2OH��CH3CH2Cl��CH3COOH�����Դ��ǣ�CH2=CH2��CH3CH2Cl��CH3COOH����2��M��X���Ҵ�������ȥ��Ӧ������ϩ����Ӧ����ʽΪCH3CH2OH ![]() CH2=CH2��+H2O���÷�ӦΪ��ȥ��Ӧ��
CH2=CH2��+H2O���÷�ӦΪ��ȥ��Ӧ��
M��WΪ�Ҵ��Ĵ�������Ӧ��������ȩ����Ӧ����ʽΪ2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O���÷�ӦΪ������Ӧ��
2CH3CHO+2H2O���÷�ӦΪ������Ӧ��
X��MΪ��ϩ��ˮ�����ļӳɷ�Ӧ�������Ҵ�����Ӧ����ʽΪCH2=CH2+H2O ![]() CH3CH2OH���÷�ӦΪ�ӳɷ�Ӧ��
CH3CH2OH���÷�ӦΪ�ӳɷ�Ӧ��
M��NΪ�������Ҵ�����������Ӧ����FΪCH3COOC2H5������ʽΪCH3COOH+CH3CH2OH ![]() CH3COOC2H5+H2O���÷�ӦΪ������Ӧ��
CH3COOC2H5+H2O���÷�ӦΪ������Ӧ��
���Դ��ǣ�CH3CH2OH ![]() CH2=CH2��+H2O����ȥ��Ӧ��
CH2=CH2��+H2O����ȥ��Ӧ��
2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O��������Ӧ��
2CH3CHO+2H2O��������Ӧ��
CH2=CH2+H2O ![]() CH3CH2OH���ӳɷ�Ӧ��
CH3CH2OH���ӳɷ�Ӧ��
CH3COOH+CH3CH2OH ![]() CH3COOC2H5+H2O��������Ӧ��
CH3COOC2H5+H2O��������Ӧ��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ġ��������Ʒ����5mol/L����0.14Lǡ����ȫ��Ӧ��������Һ�������ձ�״����2.24L������ʹ����Fe2+ȫ��ת��ΪFe3+������Ʒ���ܵĻ�ѧʽ�ǣ�������
A. Fe5O6 B. Fe3O4 C. Fe6O7 D. Fe5O7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2-����������������������Ӽ�����ͼΪʵ�����Ʊ�1��2-���������װ�Dͼ�� ͼ�з�Һ©������ƿa�зֱ�װ��ŨH2SO4����ˮ�Ҵ���dװ�D�Թ���װ��Һ�塣
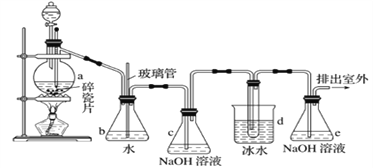
��֪����.CH3CH2OH![]() CH2=CH2��+H2O��2CH3CH2OH
CH2=CH2��+H2O��2CH3CH2OH![]() CH3CH2OCH2CH3�����ѣ�+H2O
CH3CH2OCH2CH3�����ѣ�+H2O
��.��������б����£�
�Ҵ� | 1��2-�������� | ���� | �� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� | ����ɫҺ�� |
�ܶ�/g��cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
�е�/�� | 78.5 | 131.4 | 34.6 | 58.8 |
�۵�/�� | -114.3 | 9.79 | - 116.2 | -7.2 |
ˮ���� | ���� | ���� | �� | ���� |
��1����֪����������������Ӧ�����еڶ�����Ӧ������Ӧ����Ϊ____________________��
��2��ʵ����ӦѸ�ٽ��¶����ߵ�170�����ҵ�ԭ����______________________________��
��3����ȫƿb��ʵ�����ж������á���һ���Լ��ʵ�������dװ�D�е����Ƿ�����������д����������ʱƿb�е�����_______________________________�����ʵ��ʱdװ�D�е��ܶ���������Ϊ���ܵ�ԭ����_______________________________________________����ȫƿb��������������__________________
��4������c��e�ж�ʢ��NaOH��Һ��c��NaOH��Һ��������________________________________��
��5����ȥ����������δ��Ӧ��Br2�����е���Ҫ����Ϊ___________��Ҫ��һ���ᴿ�����в����б������_____________ ������ĸ����
A���ؽᾧ B������ C������ D����ȡ
��6��ʵ����Ҳ���Գ�ȥdװ�D��ʢ��ˮ���ձ�����Ϊ����ˮֱ�Ӽ��뵽dװ�D���Թ��У����ʱ��ˮ����������ȴ1��2-��������������⣬��������������____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е��������ʲ����Ժ��ֱ�����ϣ�ֻҪ�����������ʵ���һ��������ȫȼ������O2���������ֲ������( )
A. C2H4��C2H6O B. C2H6��C2H6O C. C3H6��C2H4 D. C3H4��C2H6O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��������������ٴ��ع��������ٿ����������˿����Ӳģ�ߺ�ѧ�������ڹ�ҵ�ϳ����ø��»�ԭWO3����ȡ�����١��ش�����������
��1�����ٿ�(��Ҫ�ɷ���CaWO4)�����ᷴӦ���ɳ��������ճ������ɵõ�WO3������������Ӧ�Ļ�ѧ����ʽΪ_________________��__________________��
��2��T��ʱ��WO3�����µ��IJ���Ӧ����W��ÿһ����Ӧ���ʱ��ƽ�ⳣ�������� WO3(s)+0.1H2(g)![]() WO2.9(s)+0.1H2O(g) ��H1 K1
WO2.9(s)+0.1H2O(g) ��H1 K1
WO2.9(s)+0.18H2(g)![]() WO2.72(s)+0.18H2O(g) ��H2 K2
WO2.72(s)+0.18H2O(g) ��H2 K2
WO2.72(s)+0.72H2(g)![]() WO2(s)+0.72H2O(g) ��H3 K3
WO2(s)+0.72H2O(g) ��H3 K3
WO2(s)+2H2(g)![]() W(s)+2H2O(g) ��H4 K4
W(s)+2H2O(g) ��H4 K4
����¶�����WO3(s)+3H2(g)![]() W(s)+3H2O(g) ��H=_________��K=__________��
W(s)+3H2O(g) ��H=_________��K=__________��
��3��T1��ʱ����һ������WO3��8.0gH2����2L�ܱ���������������Ӧ�� WO3(s)+3H2(g)![]() W(s)+3H2O(g)����������������ʵ���֮����ʱ��仯�Ĺ�ϵ��ͼ��ʾ��
W(s)+3H2O(g)����������������ʵ���֮����ʱ��仯�Ĺ�ϵ��ͼ��ʾ��

��T1��ʱ��H2��ƽ��ת����a=_________%����Ӧƽ�ⳣ��K=__________��
������4minʱ���Ͳ�ά���¶�ΪT2������÷�Ӧ����H_______0������8minʱ��С������������![]() _________1.3��(����>���� <������=��)
_________1.3��(����>���� <������=��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���������������أ������й�˵���������( )
A.�ں����ȼ���м���������ʯ��,�Լ��ٶ���������ŷ���
B.Һ�����������
C.���������������ʳƷ����
D.�������Ķ�ֲ����֬����Ӧ�����Ƴ������������,���������Ϊ��ȼ��ȼ�ϵ�������������ɫ��ѧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�Ķ����ģ��ش����⣺
2017��7��9�գ��ҹ��Ϻ���ȼ���Բɹ���ȫ�����Ԥ��Ŀ�꣬��һ�ھ����Կ��ɲ������ֳ������о�����ȡ��Բ���ɹ�����5��10���������������ȡ���˶����ش�ͻ���Գɹ��������˲���ʱ���������������¼����ȼ���������ʳɷֺͽṹ�����������ɳ�Ϊ��Ȼ��ˮ������γ�������Ҫ������Դ��������ѹ��������Դ����Ҫ���д�������Ȼ��(��Ҫ�Ǽ�����)��ˮ�������ǿ�ȼ���γɵ����ʻ�����û�����ǽ��ǡ�����֮����������������Ҫ����º�ѹ��һ����Ҫ����10����¶Ⱥʹ���100������ѹ��ѹ��(ˮ��1000������)��ȱ��������������Ͳ�������췹����
���������϶��ģ��ж�����˵���Ƿ���ȷ����ԡ���������
��1����Ȼ��ȼ���Ƿ��ȷ�Ӧ��______
��2����Ȼ���ǿ�������Դ��______
��3����ȼ���γɵĻ��������ǵ��º�ѹ��______
��. ��֪��ϩ�ܷ�������ת����
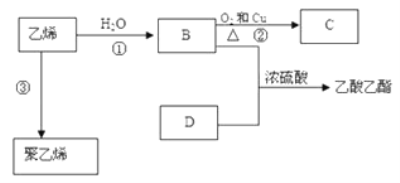
��4����ϩ�ĽṹʽΪ��___________________ ��
��5��B�����������ŵĻ�ѧʽΪ____________________��������Ϊ____________________��
��6��д�����з�Ӧ�Ļ�ѧ����ʽ��ע����Ӧ���ͣ�
��___________________________________________________����Ӧ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ��е�������Ԫ����������Ҫ��;��
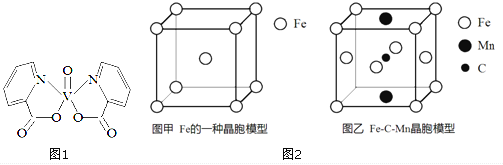
I.�о����֣���Ԫ�ص�ij����������ǿ�ȵ��ؽ������ã����ǵ����Է��ӣ��ṹ��ͼ1��
(1) ��̬VԪ�صļ۲���ӹ����ʾʽΪ___________�������зǽ���Ԫ�ص縺���ɴ�С��˳��Ϊ______________��
(2) �����в�ȡsp2�ӻ���ԭ����_________��1mol �����к�����λ������Ŀ��______��
(3) �����ʵľ����г���λ���⣬�������������������ͻ���______ (�����)��
a. ������ b.���Լ� c.�Ǽ��Լ� d.���»��� e. ���
II.Fe ��C��Mn��Ԫ�ؿ��γɶ��ֲ�ͬ���ܵĺϽ�
(4) ͼ2-����Fe��һ�־�����������Fe �Ķѻ���ʽΪ________����֪�þ�����ܶ�Ϊ��g��cm-3����NA��ʾ�����ӵ�������ֵ����þ����ı߳�Ϊ__________cm��
(5) ͼ2-����Fe-C-Mn �Ͻ�(������ȱ��)��һ�־���������Cԭ�ӵȾ����Fe �ĸ���Ϊ___���úϽ�Ļ�ѧʽΪ__________��
���𰸡�  O>N>C>H C��N 2NA bcd ���������ܶѻ�
O>N>C>H C��N 2NA bcd ���������ܶѻ� ![]() 4 Fe23Mn8C8
4 Fe23Mn8C8
��������I. (1). V��23��Ԫ�أ���۲�����Ų�ʽΪ3d34s2���۲���ӹ����ʾʽΪ ����ͼ1��֪����������к���N��O��C��H���ַǽ���Ԫ�أ���Ԫ�������ɿ�֪��������Ԫ�صķǽ�����O>N>C>H���ǽ�����Խǿ���縺��Խ����縺���ɴ�С��˳��Ϊ��O>N>C>H���ʴ�Ϊ��
����ͼ1��֪����������к���N��O��C��H���ַǽ���Ԫ�أ���Ԫ�������ɿ�֪��������Ԫ�صķǽ�����O>N>C>H���ǽ�����Խǿ���縺��Խ����縺���ɴ�С��˳��Ϊ��O>N>C>H���ʴ�Ϊ�� ��O>N>C>H��
��O>N>C>H��
(2). ��ͼ1��֪���÷����е�Cԭ�Ӻ�Nԭ�ӵĦҼ�����Ϊ3��û�йµ��Ӷԣ�����Cԭ�Ӻ�Nԭ�ӵ��ӻ������Ŀ��Ϊ3����ȡsp2�ӻ�����ͼ1��֪��V��Nԭ��֮���γ���λ����1�������к���2����λ������1mol�����к���2mol��λ������ĿΪ2NA���ʴ�Ϊ��C��N��2NA��
(3). �������ǵ����Է��ӣ�����֮����ڷ��»�������ͼ1��֪�������ʵľ����г���λ���⣬�����ڵIJ�ͬ�ǽ���ԭ��֮���γɼ��Թ��ۼ���ͬ�ַǽ���ԭ��֮���γɷǼ��Թ��ۼ��������ڽ�������������ʴ�Ϊ��bcd��
II. (4). ��Fe�ľ����ṹʾ��ͼ��֪��������Fe�Ķѻ���ʽΪ���������ܶѻ���������Feԭ�ӵĸ���Ϊ��8��![]() +1=2����������Ϊ��
+1=2����������Ϊ��![]() ��56g���辧�����ⳤΪx cm����
��56g���辧�����ⳤΪx cm����![]() ��56g=��g��cm-3��(x cm)3�����x=
��56g=��g��cm-3��(x cm)3�����x=![]() cm���ʴ�Ϊ�����������ܶѻ���
cm���ʴ�Ϊ�����������ܶѻ���![]() ��
��
(5). ��ͼ�ҿ�֪�����ĵ�Cԭ�������ĵ�Feԭ�Ӿ������������Cԭ�ӵȾ���ڵ�Feԭ�Ӹ���Ϊ4���þ�����Feԭ�Ӹ���Ϊ7��![]() +4��
+4��![]() =
=![]() ��Cԭ�Ӹ���Ϊ1��Mnԭ����ĿΪ2��
��Cԭ�Ӹ���Ϊ1��Mnԭ����ĿΪ2��![]() =1����Fe��Mn��Cԭ����Ŀ֮��Ϊ23:8:8����ѧʽΪ��Fe23Mn8C8���ʴ�Ϊ��4��Fe23Mn8C8��
=1����Fe��Mn��Cԭ����Ŀ֮��Ϊ23:8:8����ѧʽΪ��Fe23Mn8C8���ʴ�Ϊ��4��Fe23Mn8C8��
�㾦��������Ҫ�������ʽṹ�����ʣ��漰�����Ų�ʽ���縺�ԡ��ӻ���ʽ�����������ṹ���йؼ��㣬�����ѶȲ�������״����ǵ���5��С���������þ�̯�����㾧����ԭ�Ӹ���ʱ��Ҫע��þ�����ȱ�ݣ�����һ������δ����Feԭ�ӡ�
�����͡������� ����Ŀ������G��һ�ֺϳɹ�������ͼ��ʾ��
��������
12
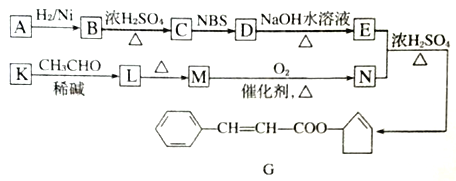
A �ķ���ʽΪC5H8O��˴Ź���������ʾ�����ַ塣������֮��Ϊ1: 1.
��֪:CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
CH3CHO+CH3CHO![]()
![]()
![]()
![]() CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
��ش���������:
(1)G�к��������ŵ�����Ϊ_______��B����C�ķ�Ӧ����Ϊ_________��
(2)A�Ľṹ��ʽΪ_______��
(3)д������ת���Ļ�ѧ����ʽ:D��E_____________________
(4)��ѧ�����飬��M��N��ת����KMnO4(H+)����O2����ʦ��Ϊ��������ԭ����_______��
(5)F��M��ͬϵ���M��һ��̼ԭ�ӡ���������������F��ͬ���칹����____�֡�(�����������칹)�����к˴Ź���������ʾ5���Ľṹ��ʽΪ_______��________��
���ܷ���������Ӧ ������������Ȼ�̼��Һ�ӳ� �۱�������2��ȡ����
(6) ��2-������NBS�Լ�Ϊԭ���Ʊ�����(������)������ƺϳ�·��(������ԭ����ѡ)__________��
�������·�ʽ��ʾ: ![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com