
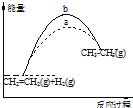
| A. | 图1的曲线说明该反应是放热反应,即CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0 | |
| B. | 化合反应都是放热反应,分解反应都是吸热反应 | |
| C. | 若图1表示有无使用催化剂时的反应进程,则b曲线使用,a曲线没使用 | |
| D. | 图中,若△H=QkJ•mol-1(Q>0),表示正反应活化能比逆反应活化能大QkJ•mol-1 |
分析 A、如图所示生成物的能量大于反应物的能量,该反应为吸热反应;
B、化和反应中碳与二氧化碳的反应为吸热反应;
C、曲线a是使用催化剂降低反应活化能的曲线;
D、依据正反应和逆反应的活化能分析判断.
解答 解:A、如图所示生成物的能量大于反应物的能量,该反应为吸热反应,故A错误;
B、化和反应中碳与二氧化碳的反应为吸热反应,故B错误;
C、依据催化剂能降低反应的活化能,图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0,a为使用催化剂反应过程中的能量变化,故B错误;
D、图象分析正逆反应的活化能之差即为该反应的焓变数值,在一定条件下,某可逆反应的△H=+100kJ•mol-1,则该反应正反应活化能比逆反应活化能大QkJ•mol-1,故D正确.
故选D.
点评 本题考查了化学反应焓变的分析判断,影响平衡因素的分析应用,注意催化剂改变反应速率的原理,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Mg在CO2中燃烧生成MgO和C,是放热反应 | |
| B. | 工业上通过电解MgCl2溶液制取金属镁 | |
| C. | Mg和稀硫酸反应时,滴加少量硫酸铜溶液,能加快反应速率 | |
| D. | 镁可以用来制造信号弹和焰火,MgO可以作耐高温材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 性质或结构信息 |
| A | 单质制成的高压灯,发出的黄光透雾力强、射程远.且其单质燃烧后生成淡黄色固体 |
| B | 工业上通过分离液态空气获得其单质.原子的最外层电子数是内层电子总数的2.5倍 |
| C | 单质是双原子分子,常温、常压下是淡黄绿色气体,原子的L层再增加一个电子即达到稳定结构 |
| D | +2价阳离子的核外电子排布与氖原子相同 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯通入酸性高锰酸钾溶液中,酸性高锰酸钾溶液褪色 | |
| B. | 在一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 | |
| C. | 在一定条件下,苯与氢气反应生成环己烷 | |
| D. | 在催化剂作用下,乙烯与水反应生成乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol碳和1 mol水蒸气反应生成1 mol CO和1 mol H2,同时吸收131.3 kJ热量 | |
| B. | 1 mol碳和1 mol水反应生成1 molCO和 1 mol H2,同时放出131.3 kJ热量 | |
| C. | 固体碳和水蒸汽反应吸收131.3 kJ热量 | |
| D. | 1个碳原子和1个水分子反应,吸热131.1 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C物质的物质的量浓度不变 | B. | 物质C和物质D的物质的量浓度相等 | ||
| C. | B物质的转化率不发生变化 | D. | 反应速率v (A)=v (D) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和Si | B. | CO2和H2O | C. | NaCl和HCl | D. | CCl4和KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物电离时,生成的阳离子是氢离子的是酸 | |
| B. | 化合物电离时,生成的阴离子是氢氧根离子的是碱 | |
| C. | 化合物电离时,生成金属阳离子和酸根离子的是盐 | |
| D. | NH4Cl的电离方程式是:NH4Cl═NH4++Cl-,NH4+不是金属阳离子,所以NH4Cl不是盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com