
37. (15分)
Ⅰ. 砷化镓为第三代半导体,以其为材料制造的灯泡寿命长.耗能少。已知砷化镓的晶胞结构如图所示。请回答下列问题:
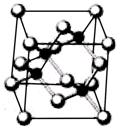
(1)下列说法正确的是__________(填序号)
A.砷化镓晶胞结构与NaCl相同 B.第一电离能 As>Ga
C.电负性 As>Ga D.原子半径 As>Ga
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为__________;
(3)AsH3空间形状为___________;已知(CH3)3 Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ. 金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因 , Cu2+的核外电子排布式为__________________________。
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有 和 。
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
15分)有机物A、D均是重要的有机合成中间体,D被称为佳味醇(chavicol),具有特殊芳香的液体,也可直接作农药使用。下图所示的是由苯酚为原料合成A、D的流程。
已知:
① (THF为一种有机溶剂)
②
③请回答下列问题:
(1)写出A、C、D的结构简式___________、_____________、_______________。
(2)是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有______种氢处于不同的化学环境。
(3)指出有机反应类型:___________。
(4)化合物B经过下列转化,可合成用于制造树脂、合成橡胶乳液的有机原料丙烯酸。
①设置反应②、⑥的目的是______________________。
②写出反应③的化学反应方程式 ___________________________。
③G与甲醇反应生成的酯H是生产丙烯酸树脂的一种重要单体,写出H聚合的化学反应方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分,每小题各3分)下图中,A到L为常见物质或该物质的水溶液,B在A气体
中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,组成J的
元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色。
回答下列问题:
(1)J的结构式为 。
(2)K的电子式为 ,属于 晶体,所含的化学键有 。
(3)若D的水溶液呈黄色,沉淀H的化学式为 。
(4)若D的水溶液呈蓝色,B与C反应的化学方程式为 。
(5)G与H2O反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(每空3分,共15分)根据下框图关系,完成下列问题:
H(白色↓)不溶于盐酸,A、B都是酸式盐。
(1)工业生产D的典型设备是 ,工业生产F选择的条件是
(2)石墨电极电解C溶液时阳极的电极方程式是
(3)B溶液中加入I溶液反应恰好显中性时的离子方程式为
(4)B溶液与A溶液反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式:(每题3分5小题共15分)
(1)石灰石溶于稀盐酸
(2)稀硫酸与氢氧化钡溶液的反应
(3)碳酸钠溶液与硝酸反应
(4)氢氧化铜与稀硫酸反应
(5)向澄清石灰水中通入少量的二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)向一个体积可变的密闭器中充入4molA、1molB,发生如下反应:
4A(g)+B(s) 3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0.3mol·L-1。
请填写下列空白:
(1)若容器体积为10L,反应经2min达平衡,则以A物质浓度变化表示的化学反应率为
。
(2)若压缩容器增大压强,则逆反应的速率 ,容器中D的体积分数 。(填“增大”“减小”“不变”)
(3)若相对分子质量M(B)>3M(C),温度升高时混合气体的平均相对分子质量减少,则正反应 。(填“吸热”或“放热”)
(4)在最初的容器改充1.5molC、4.4molD温度保持不变,要使反应达平衡时D的浓度为0.6mol·L-1,则容器的体积是 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com