

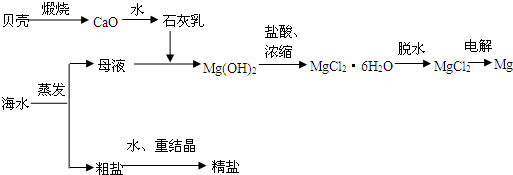
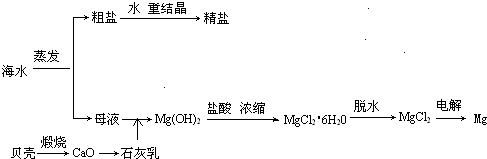
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式。
___________________________________________________________________。
(2)Mg(OH)2沉淀中混有Ca(OH)2,应怎样除去?写出实验步骤。
___________________________________________________________________。
(3)实验室里将粗盐制取精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:___________________________________________________________;
过滤时:___________________________________________________________;
蒸发时:___________________________________________________________。
解析:(1)反应物和生成物都是明确的:
□MgCl2·6H2O![]() □Mg(OH)Cl+□HCl↑+□H2O↑
□Mg(OH)Cl+□HCl↑+□H2O↑
或□MgCl2·6H2O![]() □MgO+□HCl↑+□H2O↑
□MgO+□HCl↑+□H2O↑
分别根据Mg、Cl、H(或O)原子守恒可分别配平上述两式。
(2)可使Ca(OH)2转化为Mg(OH)2,加入含Mg2+的溶液,MgCl2或Mg(NO3)2优于MgSO4,因为CaSO4微溶于水,未溶解的CaSO4能残留在Mg(OH)2中。
答案:(1)MgCl·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑;
Mg(OH)Cl+HCl↑+5H2O↑;
MgCl2·6H2O![]() MgO+2HCl↑+5H2O↑
MgO+2HCl↑+5H2O↑
(2)加入MgCl2溶液,充分搅拌,过滤,沉淀用水洗涤
(3)搅拌,加速溶解 使待滤液体沿玻璃棒流入漏斗,防止外洒 搅拌,防止因局部过热使得液体或晶体飞溅


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:

| ||
| ||
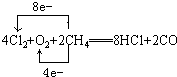
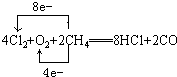
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:

(1)在空气中加热MgCl2·6H2O,假设能生成MgO和HCl,写出相应的反应的化学方程式:____________________________________________________________________。
制取金属镁时,可以用电解MgCl2的方法,写出相应的反应的化学方程式:________________________________________。
(2)电解无水氯化镁产物之一的Cl2可与空气、甲烷起反应(产物为HCl、CO),再制得盐酸循环使用,写出该反应的化学方程式并标出电子转移的方向和数目:
____________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com