
【题目】如图所示是Zn(原子量为65)和Cu形成的原电池,下列描述合理的是( )
①Zn为负极,Cu为正极 ②Cu极上有气泡产生
③阳离子移向Zn极 ④电子从Zn极流出沿导线流向Cu极
⑤该装置能将电能转化为化学能
⑥若有0.5mol电子流经导线,则负极质量减轻32.5g

A. ①②④ B. ②③ C. ④⑤⑥ D. ③④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述正确的是
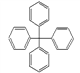
A. 此物质属于芳香烃,是苯的同系物
B. 所有碳原子可能在同一平面上
C. 常温下此分子为气态
D. 分子式为C25H20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能说明氯元素比硫元素非金属性强的是
①HC1比H2S稳定 ②HClO4酸性比H2SO4强 ③Cl2能与H2S反应生成s ④Cl2比S更易与H2化合生成相应气态氢化物 ⑤盐酸是强酸,而氢硫酸是弱酸
A. ①②③④⑤ B. ①②④⑤ C. ①②③④ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烯烃和H2O发生加成反应所得产物有同分异构体的是( )
A. CH3CH=CH2 B. CH3CH=CHCH3
C. CH2=CH2 D. (CH3)2C=C(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(13分)锰、铝、铁、钠的单质及其化合物在工业生产中有着广泛应用。请回答下列问题:
(1)工业上可用铝与软锰矿(主要成分为MnO2)反应来冶炼锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式来表示) 。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是 。
(2)将一定量的铁粉在氯气中燃烧后所得固体溶于水可得到溶液X。取少量X溶液两份,一份加入KSCN 溶液时,溶液显红色;另一份中加入黄色铁氰化钾 (K3[Fe(CN)6])溶液后能发生复分解反应生成蓝色沉淀。已知:K3[Fe(CN) 6]的电离方程式为K3[Fe(CN)6]= 3K++[Fe(CN) 6]3-。请分析:
①用化学方程式表示产生两种金属阳离子的原因 。
②蓝色沉淀是由铁氰化钾与低价态阳离子反应的结果,试写出该反应的离子方程式 。
(3)将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化。
请完成下列问题:
①反应过程中共得到的气体的体积为 (标准状况);
②最终是否有沉淀产生? (填“是”或“否”),若有沉淀产生,其质量为 。 (若不存在,则不必回答第(2)问)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com