

分析 以钛铁矿(主要成分是TiO2、少量FeO和Fe2O3)为主要原料冶炼金属钛,钛铁矿石加入硫酸,钛铁矿与硫酸发生反应的化学方程式为:FeTiO3+2H2SO4═TiOSO4+FeSO4+2H2O,所得滤液中含有TiO2+、Fe2+、Fe3+等离子,加入水溶解后加入铁防止亚铁离子被氧化,沉降分离得到溶液①,冷却结晶得到硫酸亚铁晶体,过滤得到溶液②为TiOSO4,加热过滤得到滤液为硫酸,沉淀为钛酸煅烧得到二氧化钛,加入氯气和焦炭高温反应,由二氧化钛制取四氯化钛.
(1)TiO2与酸反应生成TiO2+和水;
(2)已知TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1 2C(s)+O2(g)=2CO(g)△H=-221kJ•mol-1根据盖斯定律计算分析得到;
(3)Ⅰ.在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性;
Ⅱ.往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+;
(4)影响钛盐水解的因素有浓度、温度等,由TiOSO4水解呈酸性,知沸水、高温水蒸气、维持溶液沸腾等均为升温,沸水、高温水蒸气即加水且降低H+浓度,故高温水蒸气使水解平衡移动的作用是:加水、加热、降低H+浓度均可促进钛盐水解;
(5)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(6)利用Fe元素守恒列关系式:2FeSO4•7H2O~Fe2O3解答.
解答 解:(1)由题给反应流程可知TiO2与酸反应生成TiO2+,则反应的离子方程式为TiO2+2H+=TiO2++H2O,
故答案为:TiO2+2H+=TiO2++H2O;
(2)①TiO2 (s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2(g)═TiCl4(l)+2CO(g)△H=-81kJ•mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2(g)═TiCl4(l)+2CO(g)△H=-81kJ•mol-1;
(3)Ⅰ.在反应Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+中,氧化剂是Fe3+,氧化产物是TiO2+,所以氧化性Fe3+>TiO2+;在反应2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O中,氧化剂是TiO2+,氧化产物是Fe2+,所以氧化性TiO2+>Fe2+;在该反应中TiO2+、H+同为反应物,氧化剂是TiO2+,所以氧化性,TiO2+>H+;
所以Fe3+>TiO2+>H+,
故答案为:Fe3+;TiO2+;H+;
Ⅱ.由反应方程式可知,加入铁屑作还原剂,将Fe3+还原为Fe2+,且反应生成Ti3+保护Fe2+不被氧化.
故答案为:将Fe3+还原为Fe2+,生成Ti3+保护Fe2+不被氧化;
(4)影响钛盐水解的因素有浓度、温度等,由TiOSO4水解呈酸性,知沸水、高温水蒸气、维持溶液沸腾等均为升温,沸水、高温水蒸气即加水且降低H+浓度,故高温水蒸气使水解平衡移动的作用是:加水、加热、降低H+浓度均可促进钛盐水解,所以通入高温水蒸气的作用为:水解是吸热反应,通入高温水蒸气能降低H+浓度,提高溶液温度,促进平衡向水解方向移动,从而析出TiO2•H2O,
故答案为:水解是吸热反应,通入高温水蒸气能降低H+浓度,提高溶液温度,促进平衡向水解方向移动,从而析出TiO2•H2O;
(5)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(6)根据铁守恒2FeSO4•7H2O~Fe2O3,556akg绿矾理论上可生产Fe2O3,的物质的量为$\frac{556a×1{0}^{3}g}{278g/mol}$×$\frac{1}{2}$=1000amol,
故答案为:1000a.
点评 本题考查以钛铁矿为主要原料冶炼金属钛工艺流程,为高考常见题型,侧重于学生的分析能力、实验能力的考查,注意分析流程各反应物的转化是解答的关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z 元素的气态氢化物的热稳定性均依次递减 | |
| B. | Y、Z、W 元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | 液态WX3 气化均需克服分子间作用力 | |
| D. | 根据元素周期律,可以推测T 元素的单质具有半导体的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(加热及夹持装置省略):
实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(加热及夹持装置省略):| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g.cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
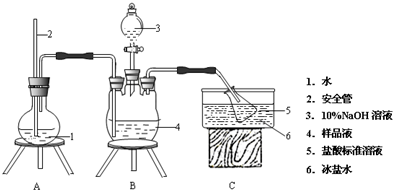
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | c | D | |
| 用 品 |  |  |  |  |
| 主要成分 | CO2 | Fe2O3 | NaHCO3 | C12H22011 |
| 用途 | 做制冷剂 | 做红色涂料 | 除油污 | 做调味剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用无水CuSO4检验酒精中是否含水 | |
| B. | 煤的干馏过程是复杂的物理和化学过程 | |
| C. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| D. | 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com