
��14�֣�ij����С��ͬѧ��ͼһװ�ý���ʵ�飬�Իش��������⡣
��1���� ����ʼʱ����K��a���ӣ������������ǵ绯ѧ��ʴ�е� ��ʴ��
�� ����ʼʱ����K��b���ӣ����ܷ�Ӧ�����ӷ���ʽ ��
��2��â������ѧʽΪNa2SO4��10H2O������ɫ���壬������ˮ����һ�ֲַ��ܹ㷺�������ο����С��ͬѧ���룬���ģ�ҵ�����ӽ���Ĥ�����ռ�ķ���������ͼ����ʾװ�õ����������Һ����ȡ������������������������ƣ����۴ӽ�ʡ��Դ�������ԭ�ϵ����������������ӷ�����ɫ��ѧ���
�� �õ��۵�������ӦʽΪ�� ����ʱͨ�������ӽ���Ĥ�������� ������ڡ���С�ڡ����ڡ���ͨ�������ӽ���Ĥ����������
�� �Ƶõ�����������Һ�ӳ��ڣ�ѡ�A������B������C������D���� ������
�� �����Ƶõ�����������������������Һ���Ϊ����ȼ�ϵ�أ����ظ����ĵ缫��ӦʽΪ ����֪H2��ȼ����Ϊ285.8 kJ/mol�����ȼ�ϵ�ع�������36 g H2Oʱ���������� kJ������ת��Ϊ���ܡ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2008?��ݸģ�⣩ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
��2008?��ݸģ�⣩ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
| ||
| ||
 ����������������������أ�
����������������������أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij����С��ͬѧ����ͼװ�ý���ʵ�飬һ��ʱ�����C�缫������ͭ�������Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬һ��ʱ�����C�缫������ͭ�������Իش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣺
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣺
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
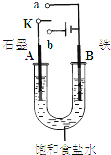 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com