
下列微粒半径大小比较正确的是( )
A.Na+<Mg2+<Al3+<O2-
B.S2->Cl->Na+>Al3+
C.Na<Mg<Al<S
D.Cs<Rb<K<Na
科目:高中化学 来源:2014年高一化学人教版必修二 2-1化学能与热能练习卷(解析版) 题型:选择题
一定量的氢气在一定条件下完全燃烧生成气态水,放出热量值为Q1,等量的H2在同样条件下完全燃烧生成液态水,放出热量值为Q2,则Q1与Q2的关系为( )
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-3-1离子键练习卷(解析版) 题型:选择题
Y元素最高正价与最低负价的绝对值之差是4;Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
A.KCl B.Na2S C.Na2O D.K2S
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-2元素周期律练习卷(解析版) 题型:选择题
下图是元素周期表的一部分,下列说法正确的是( )
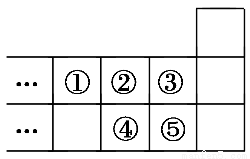
A.元素①位于第二周期第ⅣA族
B.气态氢化物的稳定性:④<②
C.最高价氧化物对应水化物的酸性:⑤<④
D.元素③的最高价是+7
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-1原子核外电子排布练习卷(解析版) 题型:填空题
有A、B、C、D四种元素,A的最高正价与其负价的绝对值之差为6;A、D次外层都是8个电子,A与D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B有两个电子层,其最高正价与最低负价的代数和为零;C2-与氩原子具有相同的电子层结构。
(1)试写出上述各元素的符号:
A________,B________,C________,D________。
(2)画出下列粒子的结构示意图:
A_________________,C2-_________________。
(3)写出A、D的最高价氧化物对应水化物反应的化学方程式:__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-1原子核外电子排布练习卷(解析版) 题型:选择题
在第n电子层中,当它作为原子的最外电子层时,能容纳的最多电子数与n-1层相同,当它作为原子的次外层时,其电子数比n+1层最多能多10个,则此电子层是( )
A.K层 B.L层 C.M层 D.N层
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-3原子结构 核素练习卷(解析版) 题型:填空题
有H、D、T三种原子,各自可形成双原子分子H2、D2、T2,请填写下列各题。
(1)标准状况下,它们的密度之比为________。
(2)相同物质的量的三种单质中,质子数之比为________。
(3)各1 g三种单质中,它们的质子数之比为________。
(4)同温同压下,1 L各单质气体中所含电子数之比为________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-2元素性质练习卷(解析版) 题型:填空题
在1961年,本生和基尔霍夫发现了一种新的碱金属元素,根据已学知道解答下列问题,帮助这两位科学家研究该元素。
(1)该元素单质的密度比水的密度大,则该元素可能是_______________________________。
(2)该元素的单质与水反应比钾与水反应剧烈,但没有铯与水反应剧烈,由此可确定该元素是________。其确定依据是_____________________________________________________。
(3)人类制备出该元素的单质比钠单质要晚得多,分析其中的原因:__________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 模块水平检测2练习卷(解析版) 题型:选择题
在恒温、恒容的密闭容器中发生反应A(g) B(g)+C(g),若反应物的浓度由2 mol/L降到0.8 mol/L需20 s,那么反应物浓度由0.8 mol/L降到0.2 mol/L所需的时间为
B(g)+C(g),若反应物的浓度由2 mol/L降到0.8 mol/L需20 s,那么反应物浓度由0.8 mol/L降到0.2 mol/L所需的时间为
A.10 s B.大于10 s C.小于10 s D.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com