
【题目】氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·H2O也是一元弱碱,25℃时电离常数Kb=4.0×10-5。现用0.0500mol/L的稀硫酸滴定l0mL 0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。下列说法正确的是

A. 甲胺在水中的电离方程式为:CH3NH2·H2O=CH3NH3++OH-
B. A、B、C三点溶液中,水电离出来的c(H+):B>C>A
C. C点所在溶液中![]()
D. B点溶液中存在c(CH3NH2·H2O)>c(CH3NH3+)>c(H+)>c(OH-)
科目:高中化学 来源: 题型:
【题目】已知钡的金属活动性处于钾和钠之间。则下列变化中可能实现的是
A. 在溶液中Ba2+可氧化金属锌,生成Zn2+ B. 钡可从硫酸铜溶液中置换出铜
C. 钡可从冷水中置换出氢气 D. 钡可从氯化钠溶液中置换出金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于各种物质的应用说法错误的是
A. 硅胶作袋装食品的吸氧剂
B. 二氧化硫作纸浆的漂白剂
C. Al(OH)3可添加到塑料中作阻燃剂
D. ClO2是一种比Cl2更安全的自来水消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝电池性能优越,Al-Ag2O2电池用于电解尿素[CO(NH2)2]的碱性溶液制备氢气(隔膜Ⅱ仅阻止气体通过,a、b均为惰性电极).下列说法正确的是( )

A. 每消耗2.7g铝,理论上a、b两极共产生气体3.36L(标准状况)
B. Ag电极是正极,反应后该电极区溶液pH减小
C. 原电池的总反应为:2Al+3Ag2O2+2NaOH=2NaAlO2+3Ag2O+H2O
D. a电极上的电极反应为:CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从植物花汁中提取的一种有机HIn,可做酸碱指示剂,在水溶液中存在电离平衡:HIn(红色) ![]() H++In-(黄色),对上述平衡解释不正确的是
H++In-(黄色),对上述平衡解释不正确的是
A.升高温度平衡向正方向移动
B.加入盐酸后平衡向逆方向移动,溶液显红色
C.加入NaOH溶液后平衡向正方向移动,溶液显黄色
D.加入NaHSO4溶液后平衡向正方向移动,溶液显黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质能相互反应得到Al(OH)3的是
A. Al跟NaOH溶液
B. Al(NO3)3跟过量的NaOH溶液
C. Al2O3和水共热
D. Al2(SO4)3和过量的氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2S(g)+O2(g)===S2(s)+2H2O(l) ΔH=-632 kJ·mol-1。下图为H2S燃料电池的示意图。下列说法正确的是
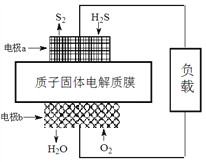
A. 电极a为电池的负极
B. 电极b上发生的电极反应为:O2+2H2O+4e-===4OH-
C. 每有1mol氧气参加反应,电池内部吸收632 kJ热能
D. 每34 g H2S参与反应,电路中有2 mol 电子通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列结论是从某同学的笔记本上摘录的,你认为其中肯定正确的是( )
①微粒半径Cl->S2->S>F ②氢化物的稳定性 HF>HCl>H2S>H2Se ③还原性S2->Cl->Br->I-④氧化性 Cl2>S>Se>Te ⑤酸性 H2SO4>HClO4>H2SeO4⑥得电子能力F>Cl>Br>I
A. 只有① B. ①③④ C. ②④⑥ D. 只有⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 常温常压下,56 g乙烯和丙烯的混合气中含有的碳原子数为4NA
B. 1.2 g NaHSO4晶体中含有的阳离子和阴离子的总数为0.03NA
C. 12 g金刚石中含有的共价键数为4NA
D. 1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com