
在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速度最快的是( )
|
| A. | V(NH3)=0.1mol/(L•min) | B. | V(N2)=0.1mol/(L•min) |
|
| C. | V(N2)=0.2mol/(L•min) | D. | V(H2)=0.3mol/(L•min) |
| 反应速率的定量表示方法. | |
| 专题: | 化学反应速率专题. |
| 分析: | 同一化学反应中,同一时间段内,各物质的反应速率之比等于其计量数之比;先把不同物质的反应速率换算成同一物质的反应速率进行比较,从而确定选项. |
| 解答: | 解:反应为N2(g)+3H2(g) A、V(NH3)=0.1mol/(L•min),所以ν(H2)=1.5mol/(L•min); B、ν(N2)=0.1mol/(L•min),所以ν(H2)=0.3mol/(L•min); C、ν(N2)=0.2mol/(L•min),所以ν(H2)=0.6mol/(L•min); D、ν(H2)=0.3mol/(L•min); 所以反应速率最快的是C. 故选C. |
| 点评: | 本题考查了化学反应速率快慢的比较,难度不大,注意要把不同物质的反应速率换算成同一物质的反应速率进行比较,还要注意单位是否相同. |


科目:高中化学 来源: 题型:
(Ⅰ)在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)═CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K==.
(2)该反应为反应(填“吸热”或“放热”).
(3)能判断该反应达到化学平衡状态的依据是BC.
A.容器中压强不变
B.混合气体中C(CO)不变
C.V(H2)正=V(H2O)逆
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:C(CO2)•C(H2)=c(CO)•c(H2O),试判断此时的温度为℃.
(Ⅱ)难溶弱电解质在水溶液中既存在溶解平衡又存在电离平衡.
已知Cu(OH)2═Cu2++2OH﹣,KSP=c(Cu2+)•2=2×l0﹣20.当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
(1)某CuSO4溶液里c(Cu2+)=0.02mol•L﹣1,如要生成Cu(OH)2沉淀,应调整沉淀pH使之大于.
(2)要使0.2mol•L﹣1CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液PH为.
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P===O c kJ·mol-1、O===O d kJ·mol-1。
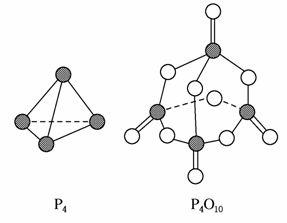
根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )
A.(6a+5d-4c-12b)kJ·mol-1
B.(4c+12d-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1
D.(4a+5d-4c-12b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
①2C(s)+O2(g)═2CO(g)△H=﹣221.0kJ/mol
②C(s)+O2(g)═CO2(g)△H=﹣393.51kJ/mol
计算反应C(s)+CO2(g)═2CO(g)的反应热△H为( )
|
| A. | +172.51 kJ/mol | B. | ﹣283.01 kJ/mol |
|
| C. | +283.01 kJ/mol | D. | +504.00 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应C(s)+H2O(g)⇌CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是( )
|
| A. | 保持体积不变,充入N2使体系压强增大 |
|
| B. | 增加C的量 |
|
| C. | 保持压强不变,充入N2使容器体积变大 |
|
| D. | 将容器的体积缩小一半 |
查看答案和解析>>
科目:高中化学 来源: 题型:
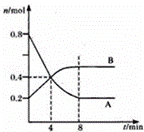
某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
(1)在4min末时,A、B的物质的量浓度c(A) c(B),从0~4min内A、B的物质的量浓度变化量△c(A) △c(B)(以上填“>”“<”或“=”).
(2)从反应开始至4min时,A的平均反应速率为 .
(3)该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子可能是
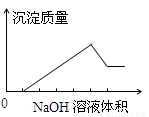
A.Mg2+、Al3+、Fe3+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.Na+、Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末考试化学试卷(解析版) 题型:选择题
S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)===SO2(g) ΔH1=-297.16 kJ·mol-1
②S(正交,s)+O2(g)===SO2(g) ΔH2=-296.83 kJ·mol-1
③S(单斜,s)===S(正交,s) ΔH3
下列说法正确的是
A.ΔH3=+0.33 kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.S(单斜, s)===S(正交,s) ΔH3<0,正交硫比单斜硫稳定
D.S(单斜,s)===S(正交,s) ΔH3>0,单斜硫比正交硫稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com