
以下表示氦原子结构的化学用语中,对电子运动状态描述最详细的是( )
A.He : B.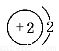 C.1s2 D.
C.1s2 D.
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:选择题
下列说法在一定条件下可以实现的是( )
①酸性氧化物与碱发生反应 ②没有水生成,也没有沉淀和气体生成的复分解反应
③弱酸与盐溶液反应可以生成强酸 ④两种酸溶液充分反应后的溶液体系为中性
⑤有单质参加的非氧化还原反应 ⑥两种氧化物反应的产物有气体
A.①②③④⑤⑥ B.②④⑤⑥ C.①②③⑤ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法不正确的是

A.可以用水代替SO(CH3)2做溶剂 B.电子移动方向是由a极流向b极
C.该装置将化学能转化为电能 D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列叙述中正确的是( )
A.主族元素的原子核外电子最后填入的能级是d能级或f能级
B.镁型和铜型金属晶体的配位数均为12
C.中心原子上的孤电子对不参与决定分子的空间结构
D.分子中键角越大,价电子对相互排斥力越大,分子越稳定
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列实验操作正确的是( )
A.在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
B.向试管中先加入一定量浓硫酸,再依次加入适量浓硝酸和苯,然后加热制取硝基苯
C.实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流
D.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置,待液体分层后,滴加硝酸银溶液
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:填空题
( 15 分)【 化学一选修化学与技术 】硫磺可用于生产化工原料硫酸。某工厂用下图所示的工艺流程生产硫酸。

请回答下列问题:
(1)为充分利用反应放出的热量,接触室中应安装 (填设备名称)。吸收塔中填充有许多瓷管,其作用是 。
(2)为使硫磺充分燃烧,经流量计1通人燃烧室的氧气过量50 % ,为提高SO2 转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计 1 和流量计 2 的空气体积比应为 。 b 管排出的尾气的处理方法 是 。
(3)与使用硫铁矿为原料的生产工艺相比,该工艺的特点是 。
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废渣减少 D.不需要使用催化剂
(4)硫酸的用途非常广,可应用于下列哪些方面 。
A.橡胶的硫化 B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产 D.过磷酸钙的制备
(5)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加人适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
一定温度下,反应 N2(g) + O2(g) 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
A.缩小体积使压强增大 B.恒容,充入N2
C.恒容,充入He D.恒压,充入He
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:实验题
工业制纯碱的第一步是通过饱和食盐水、氨和二氧化碳之间的反应,制取碳酸氢钠晶体。该反应原理可以用以下化学方程式表示,已知此反应是放热反应。
NH3+CO2+H2O+NaCl(饱和)= NaHCO3(晶体)↓+NH4Cl
(1)利用上述反应原理,设计如下图所示装置,制取碳酸氢钠晶体.B中盛有饱和碳酸氢钠溶液,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去.制取碳酸氢钠晶体可供选用的药品有:a.石灰石 b.生石灰 c.6mol/L盐酸 d.稀硫酸
e.浓氨水 f.饱和氯化钠溶液。
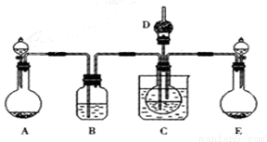
①A中制备气体时,所需药品是(选填字母代 号) ;
①B中盛有饱和碳酸氢钠溶液,其作用是 ;
③在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式为 ;
④E装置向C中通气的导管不能插入液面下的原因是 。
(2)该小组同学为了测定C中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是(选填字母序号) ;
A.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
B.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
C.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②操作Ⅲ的方法为 、 、 ;
③所得晶体中碳酸氢钠的纯度为 。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高考摸底测试理科综合化学试卷(解析版) 题型:实验题
(14分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。
(1) 160 g/L NaOH溶液的物质的量浓度为 。
(2)发生器中鼓入空气的作用可能是 (选填序号)。
a.将SO2氧化成SO3,增强酸性;
b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为 。
吸收塔的温度不能超过20℃,其目的是 。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2
外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(6) 从滤液中得到NaClO2?3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2?3H2O晶体必须进行的操作是 (填操作名称)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com