
| A.标况下22.4L水中含有的水分子数和1g H2中所含的氢气分子数 |
| B.Na2O2晶体中的阳离子和阴离子 |
| C.C原子的电子层数与最外层电子数 |
D.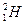 原子中的中子和质子 原子中的中子和质子 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化 合价代数和等于6 合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
 。
。 性由强到弱的顺序是 。
性由强到弱的顺序是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题: 种新型无机非金属材料,其化学式是 。
种新型无机非金属材料,其化学式是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一个D2O分子所含的中子数为8 | B.NH3的结构式为H—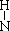 —H —H |
C.HCl的电子式为H+[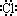 ] ] | D.热稳定性:H2S>HI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①③ | C.①④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 的是
的是 
| A.Z元素的原子半径可能比Y元素的原子半径小 |
| B.Z元素的最高化合价可能比Y元素的高 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的最高价氧化物的水化物的酸性一定比W的强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 素都是金属元素
素都是金属元素 ②④⑥ B.只有①⑥⑦ C.只有②③④ D.只有③⑤⑦
②④⑥ B.只有①⑥⑦ C.只有②③④ D.只有③⑤⑦查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com