
物质应用与其性质密切相关。下列说法错误的是
A.硅胶可防止食物受潮是由于其具有吸水性
B.葡萄糖用于医疗输液是因为它属于强电解质
C.Na2CO3可用作食用碱,因为Na2CO3的水溶液显碱性
D.酸性重铬酸钾用于检查酒驾是利用其强氧化性
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源:2016-2017学年浙江省慈溪市高二上学期期中化学试卷(解析版) 题型:选择题
下列叙述正确的是 ( )
①原电池是把化学能转化成电能的一种装置 ②原电池的正极发生氧化反应,负极发生还原反应 ③不能自发进行的氧化还原反应,通过原电池的装置均可实现 ④碳棒不能用来作原电池的正极 ⑤反应Cu+ 2Ag+=2Ag+Cu2+,能以原电池的形式来实现
2Ag+=2Ag+Cu2+,能以原电池的形式来实现
A.①⑤ B.①④⑤ C.②③④ D.②⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上期中化学试卷(解析版) 题型:填空题
已知:氮气和氢气合成氨反应为:N2(g)+3H2(g) 2NH3(g) ΔH=-92kJ/mol请回答下列问题:
2NH3(g) ΔH=-92kJ/mol请回答下列问题:
(1)取1 mo l N2(g)和3 molH2(g)充入一密闭容器中,一定条件下进行反应并达平衡时,测得反应放出的热量___________92kJ(填“大于”、“等于”或“小于”)
l N2(g)和3 molH2(g)充入一密闭容器中,一定条件下进行反应并达平衡时,测得反应放出的热量___________92kJ(填“大于”、“等于”或“小于”) ;若升高温度,上述反应中ΔH___________(填“变大”、“变小”或“不变
;若升高温度,上述反应中ΔH___________(填“变大”、“变小”或“不变 ”)。
”)。
(2)已知:分别破坏1molN H键、1mol H
H键、1mol H H键需要吸收的能量为:391 kJ、436 kJ,则破坏1mol N
H键需要吸收的能量为:391 kJ、436 kJ,则破坏1mol N N键需要吸收的能量为___________。
N键需要吸收的能量为___________。
(3)一定条件下,向体积为2L的恒容密闭容器中充入1molNH3(g) 并发生上述反应。半分钟后反应达到平衡,测得v(NH3)=0.40mol/(L•min),则N2(g)+3H2(g)  2NH3(g) 反应的平衡常数为___________。
2NH3(g) 反应的平衡常数为___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上期中化学试卷(解析版) 题型:选择题
化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是( )
A.该合成中所有的电能和热能全部转化为化学能
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市高三上学期一检化学试卷(解析版) 题型:简答题
工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸,焙烧后的矿渣用于炼铁。其转化过程如下图所示(部分条件、反应物和产物已略去):
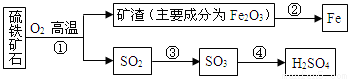
请回答下列问题:
(1)在上面转化过程中,硫元素被氧化的反应是________(填反应编号)。
(2)写出反应②中炼铁的化学方程式_____________。若用1000t含杂质28%的矿渣炼铁,理论上可得到含铁96%的生铁质量为_____________ t.
(3)写出反应①的化学方程式 ,若有12.0g FeS2参加反应,则发生转移的电子数为 。
(4)烟气中SO2的排放会造成酸雨,工业上常用Na2SO3溶液来吸收SO2以减少对环境的危害。
①常温下,将SO2通入一定体积的1.0mol·L-1Na2SO3溶液中,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,此时溶液中c(SO32-)的浓度是0.2mol·L-1,则溶液中c(HSO3-)是 mol·L-1。用化学平衡原理解释此时溶液显酸性的原因 。
②向①中pH约为6时的吸收液中通入足量O2充分反应。取反应后溶液10mL与10mLBaCl2溶液混合,欲使混合时能生成沉淀,所用BaCl2溶液的浓度不得低于 mol·L-1。[已知25℃时,Ksp(BaSO3)=5.48×10-7 , Ksp(BaSO4)= 1.08×10-10]
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市高三上学期一检化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关,下列说法正确的是
A. 煤的干馏可得到煤油、石蜡和沥青
B. 自来水厂可用明矾对水进行消毒杀菌
C. 氧化铝可用来制造耐高温的容器
D. 装有硅胶的透气袋可防止富含油脂的月饼被氧化
查看答案和解析>>
科目:高中化学 来源:2017届湖南省郴州市高三上第二次教学质量监测化学卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.NaAl(SO4)2溶液中滴加Ba(OH)2直至SO42-沉淀完全:
2Al3++ 6OH-+ 3SO42-+ 3Ba2+= 2Al(OH)3↓+3BaSO4↓
B.NH4HS溶液与少量的NaOH溶液反应:NH4++ OH-= NH3·H2O
C.稀H2SO4和Na2S2O3溶液共热:S2O32-+2H+=SO2↑+S↓+H2O
D.过量Cl2通入FeI2溶液中:3C12+2I-+ 4Fe2+= 4C1-+I2+4Fe3+
查看答案和解析>>
科目:高中化学 来源:2017届湖北省孝感市高三上第一次统考化学试卷(解析版) 题型:选择题
制备Fe3O4纳米颗粒的反应为3Fe2++ 2S2O32-+O2+xOH-=Fe3O4+S4O52-+2H2O,下列说法正确的是( )
A.x=2
B.参加反应的Fe2+全部作还原剂
C.每生成1 molFe3O4,被S2O32-还原的O2为0.5mol
D.已知Fe3O4纳米颗粒直径为20nm,则Fe3O4纳米颗粒为胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com