
根据转化关系判断下列说法正确的是( )

A.(C6H10O5)n可以是淀粉或纤维素,二者均属于多糖,互为同分异构体
B.可以利用银镜反应证明反应①的最终产物为葡萄糖
C.酸性高锰酸钾可将乙醇氧化为乙酸,将烧黑的铜丝趁热捕插乙醇中也可得到乙酸
D.在反应②得到的混合物中倒入饱和氢氧化钠溶液并分液可得到纯净的乙酸乙酯
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源:2015-2016学年山东省高一上期中测试化学试卷(解析版) 题型:选择题
下列物质的分类合理的是( )
A.电解质:CO2、Ca(OH)2、H2O、HNO3
B.碱:NaOH、Ba(OH)2、Na2CO3、NH3•H2O
C.碱性氧化物:CaO、Na2O、FeO、Mn2O7
D.盐:NH4NO3、KAl(SO4)2、NH4Cl、NaHCO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高一上期中测试化学试卷(解析版) 题型:选择题
下列反应中,属于氧化还原反应的是
A.氢氧化铝受热分解
B.氧化铜与硝酸反应
C.实验室中用高锰酸钾加热分解制取 氧气
D.实验室中用氯化铵固体与氢氧化钙固体制取氨气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第四次月考化学试卷(解析版) 题型:选择题
已知甲苯的一氯代物有4种,则甲苯与氢气完全加成后的产物的一氯代物应该具有的种类数是
A.2种 B.4种 C.5种 D.7种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上第四次月考化学试卷(解析版) 题型:选择题
为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是( )
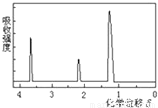
A.C2H5OH B.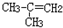
C.CH3CH2CH2COOH D.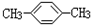
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第三次月考化学试卷(解析版) 题型:填空题
某混合物A中含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下列物质之间的变化:
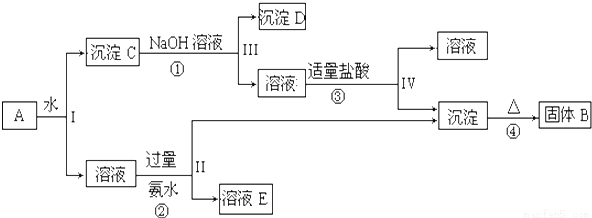
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、IV四步中对于溶液和沉淀采用的相同操作是______________。
(2)写出下列B、D、E所含物质的化学式:
固体B_______________沉淀D_______________溶液E_______________
(3)写出①、②、③、④过程中发生的三个离子反应方程式,反应④的化学方程式。
①_______________________________
②_______________________________
③_______________________________
④_______________________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第三次月考化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论错误的是
选 项 | 实验操作 | 实验现象 | 结论 |
A | 取久置的Na2O2粉末,向其中滴加过量的硫酸 | 产生无色气体 | Na2O2没有完全变质 |
B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液.再向上层溶液中滴加溴水至过量 | 实验现象1: 上层溶液不变红,下层溶液呈紫红色 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
C | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al的 |
D | 取久置的绿矾(FeSO4•7H2O)溶于水,加入KSCN溶液 | 溶液变为红色 | 绿矾部分或全部被氧化 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北邢台一中高二上学期期中测试化学试卷(解析版) 题型:选择题
下列各组微粒中不属于等电子体的是( )
A.CH4、NH4+ B.H2S、HCl C.CO2、N2O D.CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016届河南省开封市高三上学期第一次模拟理综化学试卷(解析版) 题型:实验题
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。
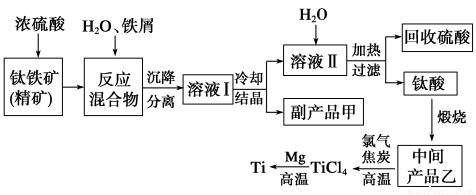
请回答下列问题。
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C===2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为______;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为_________。
(2)上述生产流程中加入铁屑的目的是___________。此时溶液中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.001 8 mol/L,当溶液的pH等于________时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为____________。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为_______。Mg还原TiCl4过程中必须在1070 K的温度下进行,你认为还应该控制的反应条件是_______。除去所得金属钛中少量的金属镁可用的试剂是______。
(4)在800~1 000 ℃时电解TiO2也可制得海绵钛,装置如下图所示。

图中b是电源的________极,阴极的电极反应式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com