
【题目】醋酸溶液中存在电离平衡CH3COOH![]() CH3COO-+H+,下列叙述正确的是( )
CH3COO-+H+,下列叙述正确的是( )
A.向溶液中加少量的CH3COONa固体或者降低温度,平衡均逆向移动,醋酸的电离常数Ka均减小
B.0.10mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)增大
C.0.10mol/LCH3COOH溶液比0.010mol/LCH3COOH溶液中c(H+)大10倍
D.室温下,欲使0.1mol/L醋酸溶液的pH、电离度α都减小,可加入少量水
【答案】B
【解析】
A.弱电解质的电离是吸热反应,降低温度抑制电离,导致电离平衡常数减小,平衡常数只与温度有关系,加少量的CH3COONa固体平衡常数不变,故A错误;
B.加水稀释促进醋酸电离,但是电离增大程度小于溶液体积增大程度,导致溶液中c(H+)减小,但是温度不变离子积常数不变,c(OH-)增大,故B正确;
C.稀释促进电离,0.10mol/LCH3COOH溶液比0.010mol/LCH3COOH溶液的电离程度小,则0.10mol/LCH3COOH溶液比0.010mol/LCH3COOH溶液中c(H+)小10倍,故C错误;
D.加水稀释促进醋酸电离,但是电离增大程度小于溶液体积增大程度,导致溶液中c(H+)减小,pH增大,故D错误;
故答案选B。


科目:高中化学 来源: 题型:
【题目】制备乙酸乙酯的绿色合成路线之一为:

下列说法不正确的是
A. M的分子式为C6H12O6 B. N的结构简式为CH3COOH
C. ④的反应类型属于取代反应 D. 淀粉与纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同质量的SO2、SO3的物质的量之比为___,所含氧原子的个数之比为____。
(2)相同条件下10mLA2气体与30mLB2气体恰好完全反应生成20mL某气体C,则C的化学式为____(用A、B表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标况下,m克气体A和n克气体B的分子数相等,下列说法正确的是
A.同体积的气体A和气体B的质量比为m:n
B.25℃时,1kg气体A和1kg气体B的分子数比为m:n
C.同温同压下,气体A和气体B的密度比为n:m
D.标准状况下,等质量的气体A和气体B的体积比为n:m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意图如下:
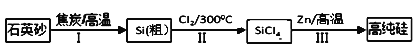
(1)1mol焦炭在过程Ⅰ中失去____mol电子。
(2)过程Ⅱ中Cl2用电解饱和食盐水制备,制备Cl2的离子方程式为________。
(3)步骤(2)中的电解过程中,若用甲醇燃料电池作电源,用KOH作电解质,负极反应为_________。
(4)整过生产过程必须严格控制无水,回答下列问题:
①SiCl4遇水剧烈水解生成SiO2和一种酸,化学反应方程式为_________。
②干燥Cl2时从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入浓H2SO4中。冷却的作用是_________。
(5)Zn还原SiCl4的可逆反应如下:
SiCl4(g)+2Zn(s)![]() Si(S)+2ZnCl2(g)△H<0下列说法正确的是(___)
Si(S)+2ZnCl2(g)△H<0下列说法正确的是(___)
A.还原过程需在无氧的气氛中进行 |
B.投入1molZn可生成14g还原产物 |
C.增加SiCl4(g)的量,该反应平衡常数不变 |
D.若SiCl4(g)过量可增大△H的值 |
(6)有一种由硅制作的材料中常加入Ag2SO4 ,已知某温度下Ag2SO4(M=312g/mol)的溶解度为0.624g/100g H2O,该温度下Ag2SO4的Ksp=_______(两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。已知多晶硅第三代工业制取流程如图所示:
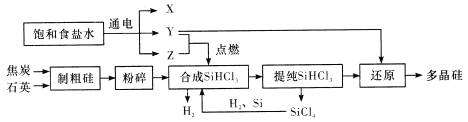
下列说法错误的是
A. Y、Z分别为H2、Cl2
B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比为1:1
C. SiHCl3极易水解,其完全水解的产物为H2SiO3、H2、HCl,据此推测SiHCl3中硅元素的化合价为+2价
D. Y与SiHCl3制备多晶硅的反应属于置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图(A)处通入Cl2,当关闭(B)阀时,(C)处的湿润的红布条没有明显变化,当打开(B)阀时,(C)处的湿润红布条逐渐褪色,则(D)瓶中装的溶液是( )

A.浓硫酸B.NaOH溶液C.水D.NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现需配制0.1mol/LNaOH溶液450mL,如图是某同学转移溶液的示意图。
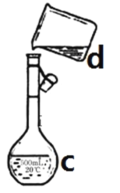
(1)写出下列仪器的名称:c.__________________
(2)图中的错误是____________________________。
(3)根据计算得知,所需NaOH的质量为____________g
(4)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)_______________。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在人类的生产和生活中有着广泛的应用,某化学兴趣小组利用图一装置探究氨气的有关性质。
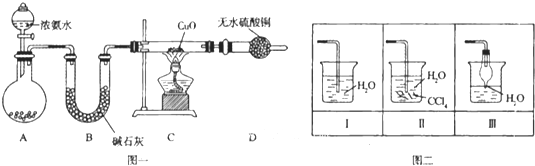
(1)装置A中烧瓶内试剂可选用 (填序号)。B的作用是
a.碱石灰 b.浓硫酸 c.生石灰 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 ,.该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为 mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com