
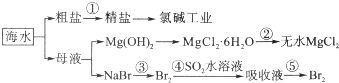
分析 海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子,可分别加热氯化钡、氢氧化钠、碳酸钠,过滤后加入盐酸,结晶得到精盐,可用于氯碱工业;母液中含有镁离子,加入氢氧化钠得到氢氧化镁,加入盐酸得到氯化镁晶体,在盐酸氛围中加热得到无水氯化镁;溴化钠中通入氯气得到溴,用二氧化硫吸收得到亚硫酸钠,继续通入氯气,得到溴,
(1)海水中的弱酸根离子水解显碱性;
(2)根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答;
(3)氯化镁易水解,为防止水解过程③中结晶出的MgCl2•6H2O要一定条件下加热脱水制得无水MgCl2;
(4)电解饱和食盐水是电能转化为化学能,惰性电极电极熔融氯化镁生成氯气和金属镁,镁和水反应生成氢氧化镁和氢气;
(5)溴离子被氧化为溴单质后,被二氧化硫吸收生成溴离子,加入氧化剂氧化溴离子为溴单质,富集溴元素;采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收利用二氧化硫还原性和溴单质反应生成硫酸和HBr.
解答 解:海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子,可分别加热氯化钡、氢氧化钠、碳酸钠,过滤后加入盐酸,结晶得到精盐,可用于氯碱工业;母液中含有镁离子,加入氢氧化钠得到氢氧化镁,加入盐酸得到氯化镁晶体,在盐酸氛围中加热得到无水氯化镁;溴化钠中通入氯气得到溴,用二氧化硫吸收得到亚硫酸钠,继续通入氯气,得到溴,
(1)海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、HCO3-等离子,在这些离子中能发生水解的是CO32-、HCO-3离子,HCO3-+H2O?H2CO3+OH-它们水解呈碱性,所以天然海水的pH≈8,呈弱碱性,
故答案为:HCO3-;
(2)镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,再进行过滤,最后再加入适量盐酸除去反应剩余的氢氧根离子和碳酸根离子,故正确的顺序为:①②④⑤,
故答案为:①②④③;
(3)镁离子水解,应抑制其水解得到无水盐,所以利用MgCl2•6H2O制得无水氯化镁,应采取的措施是在HCl气流中脱水,抑制氯化镁水解,
故答案为:在HCl气流中脱水,抑制氯化镁水解,加热至恒重;
(4)电解原理分析,电解饱和食盐水是电能转化为化学能,采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑,
故答案为:电能;化学能;MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
(5)溴离子被氧化为溴单质后,被二氧化硫吸收生成溴离子,加入氧化剂氧化溴离子为溴单质,富集溴元素,从第③步到第⑤步的目的是为了浓缩富集溴,采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收,溴单质和二氧化硫发生氧化还原反应生成硫酸和氢溴酸,发生反应的化学方程式为:Br2+SO2+2H2O=H2SO4+2HBr,
故答案为:浓缩富集溴;Br2+SO2+2H2O=H2SO4+2HBr.
点评 本题考查物质的分离、提纯,为高考常见题型,侧重于学生的分析能力、实验能力的考查,题目涉及海水资源综合利用、离子的除杂、氧化还原反应、元素及其化合物的有关知识进行综合利用,提高了试题的综合性,题目难度中等.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
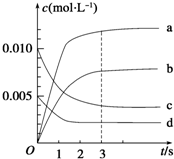 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
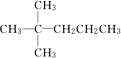 .
. 、
、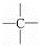 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如: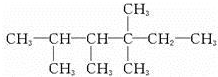
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往氯化铝溶液中滴加过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 氯气通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| C. | 往澄清石灰水中通入过量CO2:CO2+OH-=HCO3- | |
| D. | 铁粉和浓盐酸反应:Fe+2H+=Fe2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si→SiO2→H2SiO3→Na2SiO3 | B. | C→CO2→CaCO3→CO2→C | ||
| C. | Al→Al2O3→Al(OH)3→NaAlO2 | D. | FeCO3→FeO→Fe(OH)2→Fe(OH)3→Fe2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com