
����Ŀ��E��һ��������Ѫ�ܼ�����ҩ����ĺϳ�·�����£� 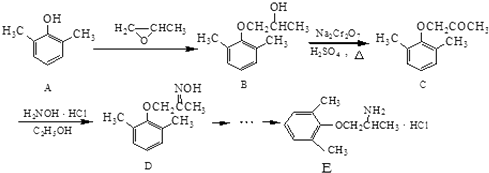
��1��C�����к��������ŵ�����Ϊ ��
��2����B��C�ķ�Ӧ����Ϊ ��
��3����A�Ʊ�B�Ĺ�����������������F������B��Ϊͬ���칹�壬F�Ľṹ��ʽΪ ��
��4��д��ͬʱ��������������D��һ��ͬ���칹��Ľṹ��ʽ�� �� �����ڦ��������
���DZ���������ұ����ϵ�һ�ȴ���ֻ�����֣�
�۷����к�����������̼ԭ�ӣ�
��5����֪��ϩ�ڴ���������������Ӧ�������ɻ������飨 ![]() ���� д�����ڼ����� ��
���� д�����ڼ����� �� 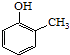 �����Ҵ�Ϊԭ���Ʊ�
�����Ҵ�Ϊԭ���Ʊ� 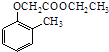 �ĺϳ�·������ͼ�����Լ����ã���
�ĺϳ�·������ͼ�����Լ����ã���
�ϳ�·������ͼʾ�����£�H2C=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH��
CH3CH2OH��
���𰸡�
��1���Ѽ����ʻ�
��2��������Ӧ
��3��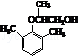
��4��![]()
��5���⣺ 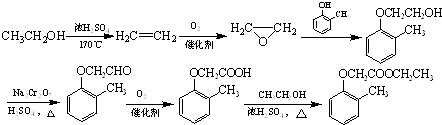
���������⣺��1���ɽṹ��ʽ��֪C�����Ѽ����ʻ������Դ��ǣ��Ѽ����ʻ�����2��B��C�ķ�Ӧ�Щ�OH����C=O��Ϊ������Ӧ�����Դ��ǣ�������Ӧ��3�� ![]() �к���2��C��O������A������Ӧʱ�������ֲ�ͬ�Ķ��ѷ�ʽ�����ɵ���һ���л���Ľṹ��ʽΪ��
�к���2��C��O������A������Ӧʱ�������ֲ�ͬ�Ķ��ѷ�ʽ�����ɵ���һ���л���Ľṹ��ʽΪ�� 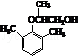 �� ���Դ��ǣ�
�� ���Դ��ǣ� 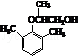 ����4��D��һ��ͬ���칹���У������ڦ�����������DZ���������ұ����ϵ�һ�ȴ���ֻ�����֣�Ӧλ�ڶ�λλ�ã��۷����к������������������������л����ͬ���칹��Ϊ��
����4��D��һ��ͬ���칹���У������ڦ�����������DZ���������ұ����ϵ�һ�ȴ���ֻ�����֣�Ӧλ�ڶ�λλ�ã��۷����к������������������������л����ͬ���칹��Ϊ�� ![]() ��
��
���Դ��ǣ� ![]() ����5���Ʊ�
����5���Ʊ�  ��Ӧ���Ʊ������
��Ӧ���Ʊ������ 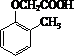 ���Ҵ��������������ᣬ�Ҵ���ȥ��������ϩ����ϩ����������
���Ҵ��������������ᣬ�Ҵ���ȥ��������ϩ����ϩ���������� ![]() ����
����  ��Ӧ����
��Ӧ����  ����������������
����������������  ����Ӧ������Ϊ
����Ӧ������Ϊ  ��
��
���Դ��ǣ�  ��
��


 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ��������������Ӧ�ù㷺�����з�Ӧ������������ԭ��Ӧ���ǣ� ��
A.ľ̿ȼ�գ�C+O2 ![]() CO2
CO2
B.����ʯ��ʯ��CaCO3 ![]() ?CaO+CO2��
?CaO+CO2��
C.����ұ����Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
D.���ˮ��2H2O ![]() 2 H2��+O2��
2 H2��+O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
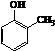
����Ŀ����ͼ��ʾ�Ƿ�������ʱ���õ��������ش��������⣺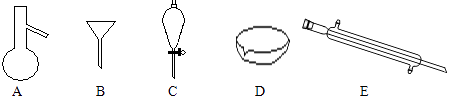
��1�������C��E��������
��2���������»����Ӧ����Ҫѡ������ʲô������������ĸ���ţ�
��NaCl�������ɳ���ڻ����ͺ�ˮ��
��3������Cװ���м����ˮ������CCl4 �� ������ã��۲쵽�����ǣ�C��Һ������㣬�ϲ�Һ��ɫ���²�Һ��ɫ��
��4���ⵥ�ʺ��嵥���������Ƶ����ʣ����������л��ܼ���ȡˮ��Һ�еĵ��ʣ�������C������ȡ��ˮ�е��嵥�ʣ������л��ܼ��в���ѡ�õ��ǣ�
A.����
B.CCl4
C.�ƾ�
D.���ᣮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п��Һ�������һ�����͵绯ѧ����װ�ã���ͼ��ʾ�������ҺΪ�廯пˮ��Һ���������Һ�ڵ���ʴ��͵�ؼ䲻��ѭ��������˵������ȷ���ǣ� �� 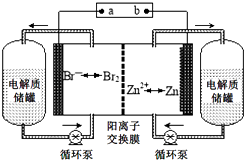
A.�����ӽ���Ĥ����ֹBr2��Znֱ�ӷ�����Ӧ
B.�ŵ�ʱ�����ĵ缫��ӦʽΪZn��2e��=Zn2+
C.���ʱ�缫a���ӵ�Դ�ĸ���
D.�ŵ�ʱ������ʴ����е�������Ũ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ�����CO2�Ի�����������Դ���������ش� 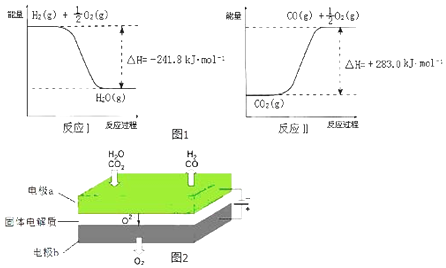
��1��Li2O��Na2O��MgO��������CO2 �� ���Ѱ������CO2���������ʣ����н���������� �� a�����ڼ�����������Ѱ��
b�����ڢ�A����A��Ԫ���γɵ���������Ѱ��
c�����ھ���ǿ�����Ե�������Ѱ��
��2�����÷�ӦA�ɽ��ͷŵ�CO2ת��Ϊ���й�ҵ���ü�ֵ�IJ�Ʒ����ӦA��CO2+H2O ![]() CO+H2+O2��֪����ͼ1��ʾ����ӦA���Ȼ�ѧ����ʽ�� ��
CO+H2+O2��֪����ͼ1��ʾ����ӦA���Ȼ�ѧ����ʽ�� ��
��3�����µ�⼼���ܸ�Чʵ�֣�3���з�ӦA������ԭ��ʾ��ͼ��ͼ2�� �ٵ缫b���������������ԭ������Ӧ��
��CO2�ڵ缫a�ŵ�ķ�Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ȩ����ϸ����Ҫ��ɲ��֣�����Ϊ���ᣨ��������3���ǻ����γɵ�������ṹ��ʽ��ͼ������˵��������ǣ� �� 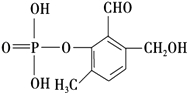
A.��������Ʒ�Ӧ
B.��ʹʯ����Һ���
C.�ܷ���������Ӧ
D.1mol������NaOH��Һ��Ӧ���������3molNaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ�ѧ����ʽ�� H2O��g��=H2��g��+ ![]() O2��g������H=+241.8kJ/mol
O2��g������H=+241.8kJ/mol
H2��g��+ ![]() O2��g��=H2O��l������H=��285.8kJ/mol
O2��g��=H2O��l������H=��285.8kJ/mol
��1gҺ̬ˮ��Ϊˮ����ʱ���������仯�ǣ� ��
A.����88 kJ
B.����44 kJ
C.����44 kJ
D.����2.44 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ���Na+��K+��Mg2+��Cu2+�������Ӽ�MnO��4��SiO2��4��AlO��2��CO2��3��HCO��3��SO2��4��Cl���������ӣ���֪���ٸ���Һ����ɫ�ھ��ⶨ��Һ��pH=12��ȡ������Һ������ϡ����[100mL��2molL��1]�����ữ���а�ɫ�������ɣ����õ�һ����ɫ��ζ�����壬������ʹ����ʯ��ˮ������������ǣ����ữ�����Һ���ˣ��õ���Һ�ף�
��1���ɢ١��ڡ��ۿ��жϣ�ԭ��Һ��һ�������ڵ������� �� һ�����ڵ������� ��
��2������Һ�ֳ����ȷݣ�һ������μ��백ˮ�������а�ɫ��״������˵��ԭ��Һ��һ�����������ӷ��ţ����տ�ʼ���백ˮʱ��û�г���������ԭ���� �� �������ӷ���ʽ��ʾ������һ���м���������Ba��NO3��2��Һ���а�ɫ�������ɣ�˵��ԭ��Һ��һ�����������ӷ��ţ������˵õ���Һ�ң�
��3������Һ���м���������AgNO3��Һ�����ˡ�ϴ�ӡ�����ù���26.5g����ԭ��Һ���Ƿ���Cl������ǡ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com