
| A�� | �ڢ� | B�� | �٢� | C�� | �ڢܢ� | D�� | �ۢ� |
���� ��ѧ��Ӧ�ﵽ��ѧƽ��״̬ʱ�����淴Ӧ������ȣ��Ҳ�����0�������ʵ�Ũ�Ȳ��ٷ����仯���ɴ�������һЩ�������������仯���Դ˽����жϣ��ó���ȷ���ۣ�
��� �⣺���淴ӦA��g��+3B��g��?2C��g��
��C������������C������������ȣ�˵����Ӧ�ﵽƽ��״̬���ʲ�ѡ��
�ڵ�λʱ��������a molA��ͬʱ����3a molB��A��B���Ƿ�Ӧ�����A��B�����ʶ����淴Ӧ���ʣ�����˵����Ӧ�ﵽƽ��״̬����ѡ��
��A��B��C��Ũ�Ȳ��ٱ仯��˵����Ӧ�ﵽƽ��״̬���ʲ�ѡ��
�ܷ�Ӧǰ�����������һֱ���䣬����������ܶ�һֱҲ���䣬����˵����Ӧ�ﵽƽ��״̬����ѡ��
�ݻ���������ѹǿ���ٱ仯����Ӧǰ�������������ͬ��ѹǿ����˵�������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬���ʲ�ѡ��
�������������ʵ������ٱ仯����Ӧǰ���������ʵ�������ͬ�����������ʵ�������˵�������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬���ʲ�ѡ��
�ߵ�λʱ������a mol A��ͬʱ����3a molB��˵�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬���ʲ�ѡ��
��A��B��C�ķ�����֮�Ⱦ����ڿ�ʼ�������ʵĶ��٣���ƽ��״̬�أ���ѡ��
��ѡC��
���� ���⿼���˻�ѧƽ��״̬���жϣ���Ŀ�ѶȲ���ע��������淴Ӧ������ȣ��Ҳ�����0�������ʵ�Ũ�Ȳ��ٷ����仯�жϣ�


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Mg��OH��2����Һ�еμ�Ũ��NH4Cl��Һ�������ܽ⣺Mg��OH��2+2H+�T2H2O+Mg2+ | |
| B�� | ��NO2��������ˮ�У���ɫ��dz2NO2 ������ɫ��g��?N2O4����ɫ��g����H��0 | |
| C�� | ������ϡ���ᣬ��Һ��ƣ�3Fe+8H++2NO3-�T3Fe2++2NO��+4H2O | |
| D�� | ������FeCl3��Һ�����ˮ����������ɫ��Fe3++3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ͼװ�ã��ش��������⣺
����ͼװ�ã��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | ��״ | �۵㣨�棩 | �е㣨�棩 | �ܶȣ�g/mL�� | �ܽ�ȣ�g�� | |
| ˮ | �Ҵ� | |||||
| �ױ� | ��ɫҺ����ȼ�ӷ� | -95 | 110.6 | 0.8669 | ���� | ���� |
| ������ | ��ɫƬ״����״���� | 122.4[1] | 248 | 1.2659 | ��[2] | ���� |
 ����Һ����ʯ�����ϼ��������ڣ�
����Һ����ʯ�����ϼ��������ڣ� +2KMnO4 $\stackrel{��}{��}$
+2KMnO4 $\stackrel{��}{��}$ +2 MnO2��+H2O+1KOH
+2 MnO2��+H2O+1KOH�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3p�������2��δ�ɶԵ��ӵ�ԭ�Ӻ�4p�������2��δ�ɶԵ��ӵ�ԭ�� | |
| B�� | 3p�������1���չ����ԭ�Ӻ�4p�������1�չ����ԭ�� | |
| C�� | ��������ֻ���������ӵļ�ԭ�Ӻ���������ֻ���������ӵ���ԭ�� | |
| D�� | ���������Ų�Ϊ3s1��ԭ�Ӻ����������Ų�Ϊ4s1��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
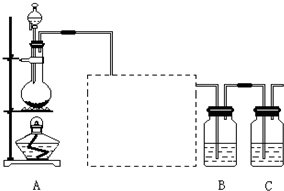
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�� | B�� | �������� | C�� | ��ˮ | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com